题目内容
13. 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:(1)电源的N端为正极;
(2)电极d上发生的电极反应式为4OH--4e-═2H2O+O2↑;
(3)当电路中有0.04mol电子通过时,a、b、c、d电极上产生的气体或固体的物质的量之比是2;2:4:1;
(4)若利用丙池实现铁上镀铜,则“e-f-x溶液”是Fe-Cu-CuSO4;(要求e、f、x用具体物质回答,下同).若利用丙池实现电解精炼铜,则“e-f-x溶液”是纯铜-粗铜-CuSO4.
分析 (1)接通电源,经过一段时间后,乙中c电极质量增加,说明c是银离子放电生成单质银,所以c是阴极,则M是负极,则N是正极;
(2)电极d是阳极,电极上发生的电极反应式为4OH--4e-═2H2O+O2↑;
(3)当电路中有0.04mol电子通过时,a是氢离子放电,生成氢气,b是氯离子放电生成氯气、c极是银离子放电生成单质银、d电极是氢氧根离子放电生成氧气,所以有0.04mol电子通过时产生的气体或固体的物质的量分别是0.02mol、0.02mol、0.04mol、0.01mol;
(4)若利用丙池实现铁上镀铜,所以e阴极是铁,f阳极是铜,电解质溶液是硫酸铜,若利用丙池实现电解精炼铜,e阴极是纯铜,f阳极是粗铜,电解质溶液是硫酸铜,由此分析解答.
解答 解:(1)接通电源,经过一段时间后,乙中c电极质量增加,说明c是银离子放电生成单质银,所以c是阴极,则M是负极,则N是正极,故答案为:正;
(2)电极d是阳极,电极上发生的电极反应式为4OH--4e-═2H2O+O2↑,故答案为:4OH--4e-═2H2O+O2↑;
(3)当电路中有0.04mol电子通过时,a是氢离子放电,生成氢气,b是氯离子放电生成氯气、c极是银离子放电生成单质银、d电极是氢氧根离子放电生成氧气,所以有0.04mol电子通过时产生的气体或固体的物质的量分别是0.02mol、0.02mol、0.04mol、0.01mol,所以a、b、c、d电极上产生的气体或固体的物质的量之比是2;2:4:1,故答案为:2;2:4:1;
(4)若利用丙池实现铁上镀铜,所以e阴极是铁,f阳极是铜,电解质溶液是硫酸铜,若利用丙池实现电解精炼铜,e阴极是纯铜,f阳极是粗铜,电解质溶液是硫酸铜,故答案为:Fe-Cu-CuSO4;纯铜-粗铜-CuSO4.
点评 本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意三个电解池为串联电路,各电极上得失电子的数目相等,做题时要正确写出电极方程式,准确判断两极上离子的放电顺序.

 全优点练单元计划系列答案
全优点练单元计划系列答案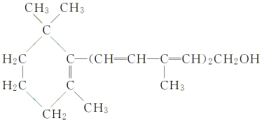
| A. | 维生素A是一种易溶于水的醇 | |
| B. | 维生素A的一个分子中含有5个碳碳双键 | |
| C. | 维生素A具有环己烷的结构单元 | |
| D. | 维生素A能发生加成、氧化、酯化等反应 |
| A. | 若铁粉有剩余,则不溶物中一定有铜 | |
| B. | 若铁粉有剩余,则溶液中的金属阳离子只有Fe2+ | |
| C. | 若铁粉无剩余,且溶液中有Cu2+,则溶液中一定无Fe3+ | |
| D. | 若铁粉无剩余,且溶液中无Cu2+,则溶液中一定有Fe2+,一定无Fe3+ |
| A. | KCl(aq),HCl(aq) | B. | HNO3(aq),KNO3(aq) | C. | HCl(aq),BaCl2(aq) | D. | NaNO3(aq),HNO3(aq) |
| A. | 石油分馏、煤的干馏均是物理变化 | |
| B. | 铅蓄电池、锂电池、碱性锌锰干电池都属于二次电池 | |
| C. | 资源的“3R”即减少消耗(Reduce)、增加重复使用(Reuse)、重复再生(Recycle)有利于实现“低碳生活” | |
| D. | PM2.5是指氮、硫的氧化物溶于水形成的酸性液体造成的空气污染 |
| A. | KClO3+6HCl═3Cl2↑+KCl+3H2O反应中还原剂与氧化剂的物质的量之比为6:1 | |
| B. | 硝酸铵受热分解的化学方程式为:5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O,在反应中被氧化与被还原的氮原子数之比为5:3 | |
| C. | 工业上制备新型净水剂高铁酸钾(K2FeO4)的一步反应如下:2FeCl3+10NaOH+3NaClO═2Na2FeO4+9NaCl+5H2O,若有2 mol FeCl3发生反应,转移电子的物质的量为6 mol | |
| D. | 氮化铝广泛应用于电子陶瓷等工业领域.在一定条件下,AlN可通过反应:Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成,方程式中AlN中氮的化合价为-3 |
| A. | I2仅是还原产物 | |
| B. | Cu(IO3)2既是氧化剂又是还原剂 | |
| C. | 氧化产物与还原产物物质的量比为13:2 | |
| D. | 当1 mol氧化剂参加反应时,被氧化的物质的物质的量为11mol |
①NH4I=NH3(g)+HI(g)
②2HI(g)=H2(g)+I2(g)
均为可逆反应,达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下反应①的平衡常数为( )
| A. | 12mol2•L-2 | B. | 16mol2•L-2. | C. | 20mol2•L-2 | D. | 25mol2•L-2 |