题目内容
5.已知NA为阿伏加德罗常数的值.有关草酸 (HOOC-COOH)的下列说法中错误的是( )| A. | 9.0g草酸中共用电子对数目为0.9NA | |
| B. | 9.0 g草酸被NaClO氧化生成CO2,转移的电子数为0.2 NA | |
| C. | 9.0 g草酸溶于水,其中C2O42-和HC2O4-的微粒数之和为0.1NA | |
| D. | 9.0g草酸受热完全分解为CO2、CO、H2O,标况下测得生成的气体体积为4.48 L |
分析 A、求出草酸的物质的量,然后根据草酸中含9对共用电子对来分析;
B、求出草酸的物质的量,然后根据由草酸被氧化为二氧化碳时,碳的化合价由+3价变为+4价;
C、草酸是二元弱酸,不能完全电离;
D、根据草酸的分解反应来计算.
解答 解:A、9g草酸的物质的量为0.1mol,而草酸中含9对共用电子对,故0.1mol草酸中含0.9NA对共用电子对,故A正确;
B、9g草酸的物质的量为0.1mol,而由草酸被氧化为二氧化碳时,碳的化合价由+3价变为+4价,故0.1mol草酸被氧化时转移0.2mol电子即0.2NA个,故B正确;
C、9g草酸的物质的量为0.1mol,但草酸是二元弱酸,不能完全电离,故草酸溶于水时,H2C2O4、C2O42-和HC2O4-的微粒个数之和为0.1NA个,故C错误;
D、草酸的分解反应为:H2C2O4$\frac{\underline{\;加热\;}}{\;}$CO2+CO+H2O,设0.1mol草酸分解生成的气体的物质的量为xmol,则有:
H2C2O4$\frac{\underline{\;加热\;}}{\;}$CO2+CO+H2O
1 2
0.1mol xmol
故有:$\frac{1}{0.1mol}=\frac{2}{xmol}$
解得x=0.2mol
故生成气体的体积为4.48L,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
13.下图中能验证氯化钠溶液(含酚酞)电解产物的装置是( )
| A. |  氢氧化钠溶液 | B. | 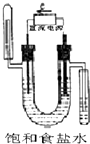 淀粉碘化钾溶液 | C. |  氢氧化钠溶液 | D. |  淀粉碘化钾溶液 |
20.下列反应的离子方程式正确的是( )
| A. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O═2OH-+H2↑+Cl2↑ | |
| B. | 向偏铝酸钠溶液中通入过量的CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| C. | 向NH4HCO3稀溶液中滴加过量Ca(OH)2溶液:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O | |
| D. | 向CuSO4溶液中滴加过量氨水:Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+ |
10.下列对于某些离子的检验及结论一定正确的是( )
| A. | 向某溶液中加入稀盐酸产生无色无味的可使澄清石灰水变浑浊的气体,则原溶液中一定含有CO32- | |
| B. | 向某溶液中加入氯化钡溶液有白色沉淀产生,再加入稀盐酸,沉淀不消失,则原溶液中一定含有SO42- | |
| C. | 向某溶液中加入碳酸钠溶液产生白色沉淀,再加入盐酸,白色沉淀消失,则原溶液中一定含有Ba2+ | |
| D. | 向某溶液中加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
17.下列物质中,分子内和分子间均可形成氢键的是( )
| A. | NH3 | B. | B | C. | H2O | D. | C2H5OH |
14.关于蛋白质的叙述中,正确的是( )
| A. | 天然蛋白质水解的最终产物都是α-氨基酸 | |
| B. | 生物催化剂“酶”是一类特殊的蛋白质,在高温时其活性强 | |
| C. | 蛋白质溶液中的蛋白质分子可透过半透膜 | |
| D. | 通过盐析作用析出的蛋白质难再溶于水 |
15.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 mol•L-1的NaClO溶液中所含ClO-的数目为NA | |
| B. | 标准状况下,2.24 L乙醇中含有的C-H数目为0.5NA | |
| C. | 常温常压下,65 g Zn与足量浓H2SO4充分反应,转移电子数一定为2NA | |
| D. | 2.24 L NO与1.12 L O2充分反应所得气体中原子数目一定为0.3NA |