题目内容
下列对电负性的理解不正确的是( )
| A、电负性是人为规定的一个相对数值,不是绝对标准 |
| B、元素电负性的大小反映了元素对键合电子引力的大小 |
| C、元素的电负性越大,则元素的非金属性越强 |
| D、元素的电负性是元素固有的性质,与原子结构无关 |
考点:元素电离能、电负性的含义及应用
专题:元素周期律与元素周期表专题
分析:A.根据电负性的标准分析,电负性是人为规定的一个相对数值,不是绝对标准;
B.根据电负性的含义分析;
C.根据电负性与元素性质的关系分析;
D.电负性用来描述不同元素的原子对键合电子吸引力的大小,与原子结构有关;
B.根据电负性的含义分析;
C.根据电负性与元素性质的关系分析;
D.电负性用来描述不同元素的原子对键合电子吸引力的大小,与原子结构有关;
解答:
解:A.根据电负性的标准:电负性是以氟为4.0、锂为1.0作为标准的相对值,电负性是人为规定的一个相对数值,不是绝对标准,故A正确;
B.根据电负性的含义,电负性用来描述不同元素的原子对键合电子吸引力的大小,故B正确;
C.元素的电负性越大,越易得电子,元素的非金属性越强,故C正确;
D.电负性用来描述不同元素的原子对键合电子吸引力的大小,与原子结构有关,同一周期电负性从左到右依次增大,故D错误;
故选D.
B.根据电负性的含义,电负性用来描述不同元素的原子对键合电子吸引力的大小,故B正确;
C.元素的电负性越大,越易得电子,元素的非金属性越强,故C正确;
D.电负性用来描述不同元素的原子对键合电子吸引力的大小,与原子结构有关,同一周期电负性从左到右依次增大,故D错误;
故选D.
点评:本题考查了电负性的含义,题目难度不大,注意根据电负性的含义进行剖析,注意掌握同周期电负性的变化规律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某学生在实验室制取乙酸乙酯(反应温度80℃左右)和乙酸丁酯(反应温度115~125℃),现有两套实验装置图Ⅰ和图Ⅱ.下列说法错误的是( )
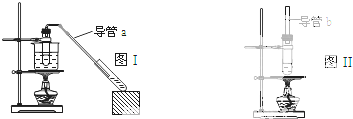

| A、制乙酸乙酯用图I装置,制乙酸丁酯用图II 装置 |
| B、导管a和导管b的作用都是冷凝回流 |
| C、都可用Na2CO3 溶液来洗去酯中的酸和醇 |
| D、加入过量的乙酸可以提高醇的转化率 |
已知某元素原子的各级电离能( kJ?mol-1)数值如下表,则该原子最外层的电子数为( )
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 577 | 1820 | 2740 | 11600 | 14800 | 18400 | 23400 |
| A、1 | B、3 | C、5 | D、7 |
下列说法正确的是( )
| A、BeCl2分子中各原子最外层均已满足8电子稳定结构 |
| B、第ⅡA族的某元素原子序数为x,则原子序数为x+1的元素不一定在第ⅢA族 |
| C、构成单质分子的粒子间一定存在化学键 |
| D、含有离子键的化合物不一定是离子化合物 |
下列分子的结构中,原子的最外层电子不能都满足8电子稳定结构的是( )
| A、HF3 |
| B、CCl4 |
| C、CO2 |
| D、PCl5 |
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
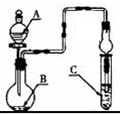

| A、若A为浓硫酸,B为铜,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛CaCl2溶液,则C中溶液变浑浊 |
| C、若A为浓盐酸,B为MnO2,C中盛KI-淀粉溶液,则C中溶液变蓝 |
| D、若A为水,B为Na2O2固体,C中盛氢硫酸溶液,则C中溶液变浑浊 |
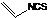 是一种天然植物杀虫剂,其中N原子的杂化方式为sp3
是一种天然植物杀虫剂,其中N原子的杂化方式为sp3