题目内容
科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.
(1)写出基态Cu原子的核外电子排布式 ;金属铜采用下列 堆积方式.
(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物.
①[Cu(NH3)4]2+中存在的化学键类型有 (填序号).
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②已知[Cu(NH3)4]2+具有对称的空间构型,若[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 .
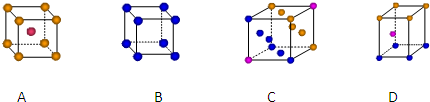
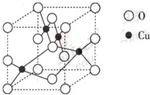
③如图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 .
(3)SO42-的VSEPR模型为 .
(1)写出基态Cu原子的核外电子排布式

(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物.
①[Cu(NH3)4]2+中存在的化学键类型有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②已知[Cu(NH3)4]2+具有对称的空间构型,若[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
③如图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为
(3)SO42-的VSEPR模型为

考点:原子核外电子排布,配合物的成键情况,晶胞的计算,不同晶体的结构微粒及微粒间作用力的区别
专题:原子组成与结构专题,化学键与晶体结构
分析:(1)Cu的原子序数为29,结合能量最低原理书写电子排布式;Cu为最密堆积,配位数为12;
(2)①配离子[Cu(NH3)4]2+中含有配位键,不同非金属元素之间形成极性共价键;
②形成4个配位键,具有对称的空间构型,可能为平面正方形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构;
③利用均摊法分析晶胞的结构;
(3)根据价层电子对互斥模型判断粒子的空间结构.
(2)①配离子[Cu(NH3)4]2+中含有配位键,不同非金属元素之间形成极性共价键;
②形成4个配位键,具有对称的空间构型,可能为平面正方形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构;
③利用均摊法分析晶胞的结构;
(3)根据价层电子对互斥模型判断粒子的空间结构.
解答:
解:(1)Cu的原子序数为29,电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1,Cu为最密堆积,配位数为12,C符合,
故答案为:1s22s22p63s23p63d104s1或[Ar]3d104s1; C;
(2)①[Cu(NH3)4]2+中Cu2+与NH3之间的化学键为配位键,N-H为极性共价键,故答案为:AC;
②形成4个配位键,具有对称的空间构型,可能为平面正方形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构,所以应为平面正方形,故答案为:平面正方形;
③从图中可以看出阴离子在晶胞有四类:顶点(8个)、棱上(4个)、面上(2个)、体心(1个),根据立方体的分摊法,可知该晶胞中阴离子数目为:8×
+4×
+2×
+1=4,故答案为:4;
(3)SO42-中中心原子S的价层电子对为
=4,孤电子对数为
=0,为正四面体结构,故答案为:正四面体.
故答案为:1s22s22p63s23p63d104s1或[Ar]3d104s1; C;
(2)①[Cu(NH3)4]2+中Cu2+与NH3之间的化学键为配位键,N-H为极性共价键,故答案为:AC;
②形成4个配位键,具有对称的空间构型,可能为平面正方形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构,所以应为平面正方形,故答案为:平面正方形;
③从图中可以看出阴离子在晶胞有四类:顶点(8个)、棱上(4个)、面上(2个)、体心(1个),根据立方体的分摊法,可知该晶胞中阴离子数目为:8×
| 1 |
| 8 |
| 1 |
| 4 |
| 1 |
| 2 |
(3)SO42-中中心原子S的价层电子对为
| 6+2 |
| 2 |
| 6+2-2×4 |
| 2 |
点评:本题考查的内容较杂,涉及到常见元素核外电子排布、金属晶体结构、配合物的结构有关知识,难度不大,注重对基础知识的考查.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、7.8g Na2O2含有的阴离子数目为0.2NA |
| B、PH=2的醋酸冲稀10倍后,溶液中H+数目大于0.001NA |
| C、25℃时,1.0L pH=9的CH3COONa溶液中H+和CH3COOH的总数目为10-5NA |
| D、己知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ?mol-1 (Q>0),则将2NA 个SO2分子和NA 个O2,分子置于一密闭容器中充分反应后放出QkJ的 热量 |
下列对电负性的理解不正确的是( )
| A、电负性是人为规定的一个相对数值,不是绝对标准 |
| B、元素电负性的大小反映了元素对键合电子引力的大小 |
| C、元素的电负性越大,则元素的非金属性越强 |
| D、元素的电负性是元素固有的性质,与原子结构无关 |
下列研究分析方法正确的是( )
| A、分别测定SO2、CO2饱和溶液的PH,可比较H2SO3、H2CO3二酸的强弱 |
| B、先滴入少量氯水,后滴入KSCN试液,可确定溶液中是否含Fe2+ |
| C、25℃若测知氨水与NH4Cl混合溶液的pH>7,可确定溶液中c(NH4+)>c(Cl-) |
| D、固体NH2COONH4(s)在密闭容器中存在:NH2COONH4(s)?2NH3(g)+CO2(g)△S>0,由此可确定反应的△H<0 |
下列依据相关实验得出的结论正确的是( )
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、用铂丝蘸取少量某溶液进行颜色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| C、Al、Fe、Cu对应的氧化物均能与酸反应生成盐和水,三种金属的氧化物均为碱性氧化物 |
| D、向某溶液中滴加氯水后,再滴加KSCN溶液后溶液显血红色,该溶液中不一定含Fe2+ |
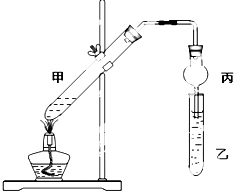 如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓慢加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸.将试管甲固定在铁架台上,在试管乙中加入5mL饱和碳酸钠溶液,按如图连接好装置进行实验,当试管乙中有明显现象时停止实验.
如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓慢加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸.将试管甲固定在铁架台上,在试管乙中加入5mL饱和碳酸钠溶液,按如图连接好装置进行实验,当试管乙中有明显现象时停止实验.