题目内容
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
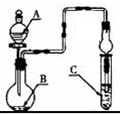

| A、若A为浓硫酸,B为铜,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛CaCl2溶液,则C中溶液变浑浊 |
| C、若A为浓盐酸,B为MnO2,C中盛KI-淀粉溶液,则C中溶液变蓝 |
| D、若A为水,B为Na2O2固体,C中盛氢硫酸溶液,则C中溶液变浑浊 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.铜与浓硫酸反应需要加热才会生成SO2;
B.二氧化碳与氯化钙溶液不反应;
C.MnO2与浓盐酸反应需要加热才会生成Cl2,没有Cl2生成;
D.过氧化钠与水反应生成氧气,氧气可氧化硫化氢.
B.二氧化碳与氯化钙溶液不反应;
C.MnO2与浓盐酸反应需要加热才会生成Cl2,没有Cl2生成;
D.过氧化钠与水反应生成氧气,氧气可氧化硫化氢.
解答:
解:A.铜与浓硫酸反应需要加热才会生成SO2,没有SO2生成,所以C溶液无现象,故A错误;
B.醋酸酸性强于碳酸,醋酸和碳酸钙反应生成二氧化碳,通入CaCl2溶液不反应,C中无现象,故B错误;
C.MnO2与浓盐酸反应需要加热才会生成Cl2,没有Cl2生成,故C错误;
D.过氧化钠与水反应生成氧气,氧气可氧化硫化氢,C中溶液有硫生成,变浑浊,故D正确.
故选D.
B.醋酸酸性强于碳酸,醋酸和碳酸钙反应生成二氧化碳,通入CaCl2溶液不反应,C中无现象,故B错误;
C.MnO2与浓盐酸反应需要加热才会生成Cl2,没有Cl2生成,故C错误;
D.过氧化钠与水反应生成氧气,氧气可氧化硫化氢,C中溶液有硫生成,变浑浊,故D正确.
故选D.
点评:本题考查了常见气体制备原理的应用和性质验证,侧重于学生分析能力和实验能力的考查,掌握它们的反应原理是解答的关键,题目难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列对电负性的理解不正确的是( )
| A、电负性是人为规定的一个相对数值,不是绝对标准 |
| B、元素电负性的大小反映了元素对键合电子引力的大小 |
| C、元素的电负性越大,则元素的非金属性越强 |
| D、元素的电负性是元素固有的性质,与原子结构无关 |
下列研究分析方法正确的是( )
| A、分别测定SO2、CO2饱和溶液的PH,可比较H2SO3、H2CO3二酸的强弱 |
| B、先滴入少量氯水,后滴入KSCN试液,可确定溶液中是否含Fe2+ |
| C、25℃若测知氨水与NH4Cl混合溶液的pH>7,可确定溶液中c(NH4+)>c(Cl-) |
| D、固体NH2COONH4(s)在密闭容器中存在:NH2COONH4(s)?2NH3(g)+CO2(g)△S>0,由此可确定反应的△H<0 |
下列依据相关实验得出的结论正确的是( )
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、用铂丝蘸取少量某溶液进行颜色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| C、Al、Fe、Cu对应的氧化物均能与酸反应生成盐和水,三种金属的氧化物均为碱性氧化物 |
| D、向某溶液中滴加氯水后,再滴加KSCN溶液后溶液显血红色,该溶液中不一定含Fe2+ |
下列说法正确的是( )
| A、100mL1mol/L Al2(SO4)3溶液中,Al3+数为0.2×6.02×1023 |
| B、0.1mol锌与100mL1mol/L 的稀盐酸充分反应,产生氢气的分子数为0.1×6.02×1023 |
| C、C60和C70的混合物共12g,其中所含碳原子数为6.02×1023 |
| D、1mol甲基(-CH3)与1mol氢氧根(OH-)所含电子数均为10×6.02×1023 |
下列有关表达正确的是( )
| A、硫离子的电子排布式:1s22s22p63s23p4 |
B、H2O的电子式: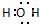 |
C、N原子最外层电子的轨道表示式: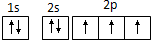 |
D、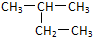 的名称:2-乙基丙烷 的名称:2-乙基丙烷 |
 实验室制得气体中常含有杂质,影响其性质检验.如图A为除杂装置,B为性质检验装置,完成下列表格:
实验室制得气体中常含有杂质,影响其性质检验.如图A为除杂装置,B为性质检验装置,完成下列表格:
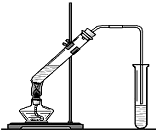 (1)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
(1)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止