题目内容
6.下列物质:①Cl2 ②HBr ③H2O ④H2,其中在一定条件下能与乙烯发生加成反应的是( )| A. | ①② | B. | ③④ | C. | ①③④ | D. | 全部 |
分析 乙烯中含碳碳双键,可发生加成反应,以此来解答.
解答 解:乙烯含碳碳双键,在一定条件下分别与①Cl2 ②HBr ③H2O ④H2发生加成反应生成1,2-二氯乙烷、溴乙烷、乙醇、乙烷,
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握烯烃的加成反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列有关物质性质的应用不正确的是( )
| A. | 常温下浓硫酸能使铝发生钝化,可在常温下用铝制贮藏罐贮运浓硫酸 | |
| B. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| C. | 次氯酸具有强氧化性,因此氯气可用于自来水的杀菌消毒 | |
| D. | 液氨汽化时要吸收大量的热,可用作制冷剂 |
14.下列有关除杂质(括号中为杂质)的操作中,错误的是( )
| A. | 溴乙烷(乙醇):多次加水振荡,分液,弃水层 | |
| B. | 苯(苯酚):加溴水,振荡,过滤除去沉淀 | |
| C. | 溴苯(溴单质):加NaOH溶液振荡,分液,弃水层 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层 |
1.表是元素周期表的一部分,回答下列有关问题:
(1)画出原子的结构示意图:④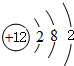 ,⑧
,⑧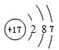
(2)第三周期(除稀有气体元素)中原子半径最大的元素是③(填序号),跟它同周期原子半径最小的元素是⑧(填序号)
(3)元素⑦与元素⑧相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)写出实验室制取元素①的气态氢化物最常用的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(5)元素①的最高价氧化物对应的水化物的浓溶液与单质铜反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
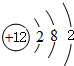 ,⑧
,⑧
(2)第三周期(除稀有气体元素)中原子半径最大的元素是③(填序号),跟它同周期原子半径最小的元素是⑧(填序号)
(3)元素⑦与元素⑧相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)写出实验室制取元素①的气态氢化物最常用的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(5)元素①的最高价氧化物对应的水化物的浓溶液与单质铜反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
11.能用于除去甲烷中混有的乙烯的试剂是( )
| A. | 溴水 | B. | 酸性高锰酸钾溶液 | ||
| C. | 苛性钠溶液 | D. | 四氯化碳溶液 |
18.下列有关如图装置的说法正确的是( )
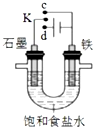

| A. | 若K与c连接,石墨电极的电极反应为:O2+4e-+4H+=2H2O | |
| B. | 若K与c连接,则溶液中的Na+向铁电极移动 | |
| C. | 若K与d连接,铁电极的电极反应为:2H++2e-═H2↑ | |
| D. | 若K与d连接,一段时间后,加适量稀盐酸可使电解质溶液复原 |
16.下列叙述中,不正确的是( )
| A. | 2H与3H互为同位素 | B. | 金刚石与石墨互为同素异形体 | ||
| C. | 3O2$\frac{\underline{\;放电\;}}{\;}$2O3是物理变化 | D. | 乙醇与二甲醚互为同分异构体 |