题目内容
16.在0.01mol•L-1的BaCl2溶液中,加入体积相同的2.0×10-4mol•L-1的Na2CO3溶液,是否有沉淀生成?(此温度下,Ksp(BaCO3)=8.1×10-9)分析 先计算出两溶液混合后钡离子和碳酸根离子的浓度,然后计算出浓度商,将计算结果与Ksp(BaCO3)=8.1×10-9比较,可判断混合液中是否有碳酸钡沉淀生成.
解答 解:在0.01mol•L-1的BaCl2溶液中,加入体积相同的2.0×10-4mol•L-1的Na2CO3溶液,
混合液中的浓度商为:c(CO32-)•c(Ba2+)=0.005×1.0×10-4=5×10-7>8.1×10-9,
所以两溶液混合后会生成碳酸钡沉淀,
答:两溶液混合后会生成BaCO3沉淀.
点评 本题考查了难溶物溶度积的计算,题目难度中等,明确难溶物溶解平衡及其影响为解答关键,注意掌握溶度积的表达式及应用方法,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
6.下列有关表达式中不正确的是( )
| A. | 乙烷的电子式: | B. | 乙烯的结构式: | ||
| C. | 乙醇的实验式:CH3O | D. | 乙酸的结构简式:CH3COOH |
7.短周期元素W、X、Y、Z的原子序数依次增大,且质子数之和为36.它们可组成离子化合物Y2X和共价化合物ZX3,已知X、Z同主族,下列说法正确的是( )
| A. | 离子半径:Y>Z>X | |
| B. | 阴离子的还原性:W>Z | |
| C. | W和其他3种元素均能形成共价化合物 | |
| D. | X、Y、Z三种元素组成的化合物水溶液一定显碱性 |
4.已知甲酸的酸性比乙酸强,那么相同温度下( )
| A. | 甲酸溶液中水的离子积Kw比乙酸强 | |
| B. | c(酸)相同时,甲酸的导电性比乙酸强 | |
| C. | c(H+)相同时,乙酸的物质的量浓度比甲酸大 | |
| D. | c(酸)相同时,甲酸溶液的pH比乙酸大 |
11.下列说法正确的是( )
| A. | 石油是多种烃的混合物,只含碳、氢两种元素 | |
| B. | 石油分馏得到的各馏分为纯净物 | |
| C. | 石油裂解的主要目的是为了提高汽油的产量 | |
| D. | 裂化汽油中含烯烃,不易作卤素单质的萃取剂 |
4.用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取4.1g烧碱样品,所用主要仪器是托盘天平、药匙、烧杯.
(2)将样品配成250mL待测液,需要的仪器有烧杯、玻璃棒、250ml容量瓶、胶头滴管.
(3)取10.00mL待测液,用碱式滴定管量取.
(4)用0.2010mol•L-1标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶中溶液颜色的变化,直到滴定终点.
(5)根据下列数据,计算待测烧碱的纯度:97.56%.
(6)在滴定操作中,导致实验结果偏低的是②⑤
①酸式滴定管用蒸馏水洗净后没有用标准液润洗
②酚酞指示剂变色时立即停止滴定
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确.
(1)准确称取4.1g烧碱样品,所用主要仪器是托盘天平、药匙、烧杯.
(2)将样品配成250mL待测液,需要的仪器有烧杯、玻璃棒、250ml容量瓶、胶头滴管.
(3)取10.00mL待测液,用碱式滴定管量取.
(4)用0.2010mol•L-1标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶中溶液颜色的变化,直到滴定终点.
(5)根据下列数据,计算待测烧碱的纯度:97.56%.
| 滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
①酸式滴定管用蒸馏水洗净后没有用标准液润洗
②酚酞指示剂变色时立即停止滴定
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确.
11.用中和滴定法测定烧碱的纯度(烧碱中的杂质不和酸反应),请根据实验回答
(1)将称量好的8.8g烧碱样品配制成500mL待测液,配制过程使用的主要仪器除500mL容量瓶、量筒、烧杯、胶头滴管外,还有一种必须使用的仪器是玻璃棒.
(2)用碱式滴定管量取10.00mL待测液于锥形瓶中,滴入几滴酚酞.
(3)用0.20mol•L-1的标准盐酸滴定待测液,判断滴定终点的现象是:当滴入最后一滴盐酸,溶液由红色变为无色,且半分钟内不褪色.
(4)如果实验操作正确,从滴定开始到结束,溶液中的离子浓度关系可以出现的是BC(填答案字母序号)
A.c(Na+)>c(Cl-)>c(H+)>c(OH-)
B.c(Na+)>c(OH-)>c(Cl-)>c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(Cl-)
D.c(Cl-)+c(Na+)>c(OH-)+c(H+)
(5)根据下列数据计算,c(NaOH)0.40mol/L
(6)经过分析发现,本次实验的测定结果比烧碱的实际纯度偏高,造成误差的可能原因是BCD
A.滴定前平视,滴定后俯视
B.未用标准液润洗滴定管
C.用待测液润洗锥形瓶
D.不小心将标准液滴在锥形瓶外面.
(1)将称量好的8.8g烧碱样品配制成500mL待测液,配制过程使用的主要仪器除500mL容量瓶、量筒、烧杯、胶头滴管外,还有一种必须使用的仪器是玻璃棒.
(2)用碱式滴定管量取10.00mL待测液于锥形瓶中,滴入几滴酚酞.
(3)用0.20mol•L-1的标准盐酸滴定待测液,判断滴定终点的现象是:当滴入最后一滴盐酸,溶液由红色变为无色,且半分钟内不褪色.
(4)如果实验操作正确,从滴定开始到结束,溶液中的离子浓度关系可以出现的是BC(填答案字母序号)
A.c(Na+)>c(Cl-)>c(H+)>c(OH-)
B.c(Na+)>c(OH-)>c(Cl-)>c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(Cl-)
D.c(Cl-)+c(Na+)>c(OH-)+c(H+)
(5)根据下列数据计算,c(NaOH)0.40mol/L
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.60 | 20.50 |
| 第二次 | 10.00 | 3.00 | 23.10 |
A.滴定前平视,滴定后俯视
B.未用标准液润洗滴定管
C.用待测液润洗锥形瓶
D.不小心将标准液滴在锥形瓶外面.
8.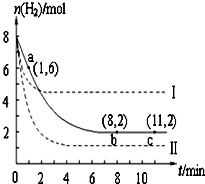 T℃时,将6mol CO2和8mol H2充入2L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )
T℃时,将6mol CO2和8mol H2充入2L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )
 T℃时,将6mol CO2和8mol H2充入2L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )
T℃时,将6mol CO2和8mol H2充入2L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )| A. | T℃时,该反应的化学平衡常数为0.125 | |
| B. | 若曲线Ⅰ对应的条件改变是升温,则该反应?△H>0 | |
| C. | 曲线Ⅱ对应的条件改变是降低压强 | |
| D. | 反应开始至a点时v(H2)=1 mol•L-1•min-1 |
9.下列有关电解质的说法正确的是( )
| A. | 强电解质的溶液一定比弱电解质的溶液导电性强 | |
| B. | 易溶性强电解质的溶液中不存在溶质分子 | |
| C. | 强电解质都是离子化合物,而弱电解质都是共价化合物 | |
| D. | 由于硫酸钡难溶于水,所以是弱电解质 |