题目内容
4.已知甲酸的酸性比乙酸强,那么相同温度下( )| A. | 甲酸溶液中水的离子积Kw比乙酸强 | |
| B. | c(酸)相同时,甲酸的导电性比乙酸强 | |
| C. | c(H+)相同时,乙酸的物质的量浓度比甲酸大 | |
| D. | c(酸)相同时,甲酸溶液的pH比乙酸大 |
分析 A、温度一定水的离子积是一个常数;
B、导电性强说明离子浓度大;
C、c(H+)相同时,乙酸的电离度小于甲酸;
D、氢离子浓度越大PH值越小.
解答 解:A、水的离子积是温度的函数,温度一定水的离子积一定,与水的强弱无关,故A错误;
B、导电性强说明离子浓度大,而甲酸和乙酸都是一元酸,所以甲酸的电离程度大,故B正确;
C、c(H+)相同时,乙酸的电离度小于甲酸,所以c(H+)相同时,乙酸的物质的量浓度比甲酸大,故C正确;
D、氢离子浓度越大PH值越小,所以c(酸)相同时,甲酸溶液的pH比乙酸小,故D错误;
故选BC.
点评 本题考查了弱电解质的判断,熟悉电解质强弱的概念、熟悉水的离子积是温度的函数是解题关键,题目难度中等.

练习册系列答案
相关题目
14.下列实验数据合理的是( )
| A. | 用托盘天平称取11.70g食盐 | |
| B. | 用量筒量取20.00mL未知浓度的盐酸注入锥形瓶 | |
| C. | 用标准NaOH溶液滴定未知浓度的盐酸,用去20.10mL NaOH溶液 | |
| D. | 用广泛pH试纸测某溶液的pH=3.5 |
12.25℃时某0.1mol/L的一元弱酸(用HA表示),未电离的弱酸分子(HA)的物质的量与电离生成的阴、阳离子总物质的量之比为4.5:1,则此溶液( )
| A. | 电离度α为10% | B. | α=20% | ||
| C. | pH=1 | D. | c(OH-)=1×10-12mol/L |
19.在相同温度下,体积相等且pH均等于3的盐酸和醋酸溶液,分别加蒸馏水稀释100倍后,下列分析中正确的是( )
| A. | 二者的pH仍然相等且均为5 | B. | 盐酸的pH大 | ||
| C. | 醋酸的pH大 | D. | 盐酸的pH为5,醋酸的pH在3~5之间 |
9.对于有气体参加的化学反应,下列说法正确的是( )
| A. | 增大压强,活化分子百分数增大,化学反应速率一定增大 | |
| B. | 升高温度,活化分子百分数增大,化学反应速率一定增大 | |
| C. | 加入反应物,活化分子百分数增大,化学反应速率增大 | |
| D. | 使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率一定增大 |
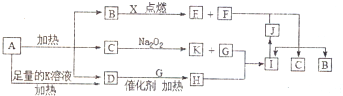
 ,写出F的一种同素异形体金刚石(C60、石墨等),D分子的空间构型为三角锥形.
,写出F的一种同素异形体金刚石(C60、石墨等),D分子的空间构型为三角锥形.