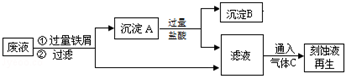
题目内容
7.碳酸氢铵溶液和过量Na(OH)溶液反应:NH4++HCO3-+2OH-═NH3.H2O+CO32-+H2O.分析 二者反应生成碳酸钠、一水合氨和水,其中少的要符合组成之比,由此分析解答.
解答 解:碳酸氢铵溶液和过量NaOH溶液反应生成碳酸钠、一水合氨和水,离子方程式为NH4++HCO3-+2OH-═NH3.H2O+CO32-+H2O,故答案为:NH4++HCO3-+2OH-═NH3.H2O+CO32-+H2O.
点评 本题考查了离子方程式的书写,明确物质之间的反应及离子方程式书写规则即可解答,注意反应物的量有关,为易错点.

练习册系列答案
相关题目
17.下列实验操作中错误的是( )
| A. | 蒸发结晶操作时,当有大量晶体析出时停止加热,用余热蒸干 | |
| B. | 蒸馏操作时,应使温度计水银球插入液态混合物中 | |
| C. | 分液操作时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 | |
| D. | 萃取操作时,萃取剂要和原溶剂互不相溶,且不能与溶质和溶剂反应 |
19.乙醇和二甲醚在下列哪一种检测仪上显示出的信号是完全相同的( )
| A. | 质谱仪 | B. | 红外光谱仪 | C. | 元素分析仪 | D. | 核磁共振仪 |
 .
. ,C的最高价氧化物水化物的电子式
,C的最高价氧化物水化物的电子式 ,淡黄色的固体E的电子式
,淡黄色的固体E的电子式 .
.
 .
. .
.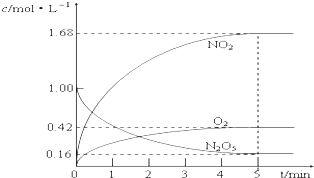 (1)该反应的化学方程式为2N2O5?4NO2+O2
(1)该反应的化学方程式为2N2O5?4NO2+O2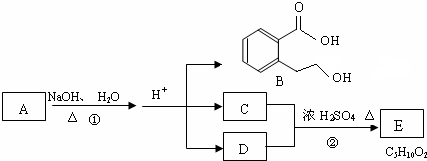
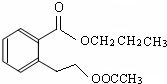 或
或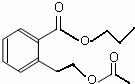 .
. .
.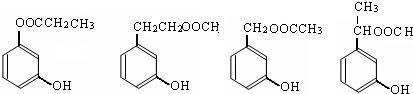 (写出四者之一即可).
(写出四者之一即可).