题目内容
12.写出下列烷烃:分子中有26个电子的结构简式CH3CH2CH3.分子中含25个化学键的分子式C8H18,支链含乙基的烷烃中相对分子质量最小的物质名称是3-乙基戊烷,C8H18分子中有三个甲基的同分异构体4种.
分析 由烷烃通式CnH2n+2可知,
分子中有26个电子,则6n+2n+2=26,解得n=3;
分子中含25个化学键,则n-1+2n+2=25,n=8;
支链含乙基的烷烃中相对分子质量最小,则主链含5个C,3号C上有乙基;
C8H18分子中有三个甲基,主链含7个C,只有1个支链(甲基)或主链含6个C,只有1个支链(-CH2CH3).
解答 解:由烷烃通式CnH2n+2可知,
分子中有26个电子,则6n+2n+2=26,解得n=3,为丙烷,其结构简式为CH3CH2CH3;
分子中含25个化学键,则n-1+2n+2=25,n=8,分子式为 C8H18;
支链含乙基的烷烃中相对分子质量最小,则主链含5个C,3号C上有乙基,烷烃名称为3-乙基戊烷;
C8H18分子中有三个甲基,若支链为-CH3,主链含有7个碳原子,符合条件有3种:CH3CH(CH3)CH2CH2CH2CH2CH3,CH3CH2CH(CH3)CH2CH2CH2CH3,CH3CH2CH2CH(CH3)CH2CH2CH3;
若支链为-CH2CH3,主链含有6个碳原子,符合条件有种:CH3CH2CH2CH(CH2CH3)2;
若支链为-CH2CH2CH3,主链含有5个碳原子,-CH2CH2CH3至少在4号碳上,无此结构,故符合条件的烷烃有4种.
故答案为:CH3CH2CH3; C8H18; 3-乙基戊烷; 4.
点评 本题考查有机物分子式计算的确定,为高频考点,把握烷烃的通式、结构及同分异构体推断为解答的关键,侧重分析与应用能力的考查,注意通式法应用,题目难度不大.

练习册系列答案
相关题目
3.恒温恒容密闭容器中,能够表明反应A(s)+3B(g)?2C(g)+D(g)已达平衡的是( )
①混合气体的压强不变;
②混合气体的密度不变;
③B的物质的量浓度不变;
④容器内B、C、D三种气体的浓度比为3:2:1;
⑤混合气体的相对分子质量不变;
⑥消耗3molB的同时生成2molC.
①混合气体的压强不变;
②混合气体的密度不变;
③B的物质的量浓度不变;
④容器内B、C、D三种气体的浓度比为3:2:1;
⑤混合气体的相对分子质量不变;
⑥消耗3molB的同时生成2molC.
| A. | ①②③ | B. | ②③④ | C. | ②③⑤ | D. | ①③⑥ |
20.下列各组两种微粒间的关系与${\;}_{1}^{3}$H、${\;}_{1}^{2}$H之间关系相同的是( )
| A. | ${\;}_{8}^{18}$O,${\;}_{8}^{17}$O | B. | O2,O3 | C. | Fe3+,Fe2+ | D. | ${\;}_{6}^{12}$C,${\;}_{6}^{13}$C |
4.元素的性质随着原子序数的递增呈现周期性变化的原因是( )
| A. | 元素原子的核外电子排布呈周期性变化 | |
| B. | 元素原子的最外层电子排布呈周期性变化 | |
| C. | 元素的化合价呈周期性变化 | |
| D. | 元素原子半径呈周期性变化 |
1.下列因果关系叙述正确的是( )
| A. | 浓HNO3的氧化性比稀HNO3,故有时在实验室看到的浓硝酸呈黄色 | |
| B. | Na的金属性比Mg强,故可用Na与MgCl2溶液反应制取Mg | |
| C. | Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中Fe也显+3价 | |
| D. | AlCl3易水解,故由AlCl3•6H2O制无水AlCl3应在HCl气流中加热 |
19.某芳香烃的分子式为C11H16,分子结构中只含有一个烷基,符合条件的烃有( )
| A. | 8种 | B. | 7种 | C. | 5种 | D. | 4种 |
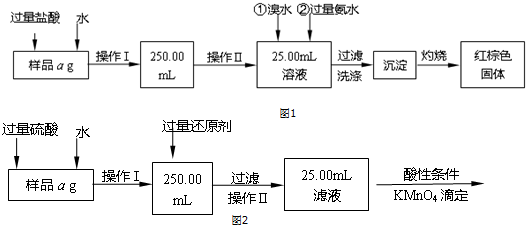
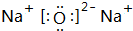 、
、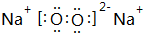 .
.