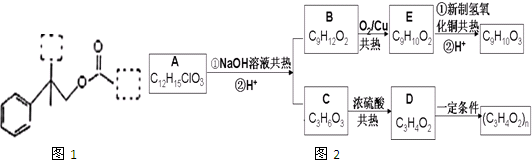
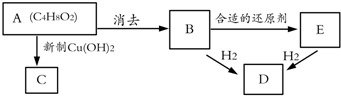
题目内容
下列各组离子一定能大量共存的是( )
| A、醋酸溶液中:K+、Cu2+、Na+、C1-、SO42- | ||
| B、pH=ll的溶液中:HCO3-、Na+、NH3.H2O、NO3- | ||
C、常温下,
| ||
| D、在含有大量Fe3+的溶液中:A13+、Na+、S2-、Br- |
考点:离子共存问题
专题:离子反应专题
分析:A.K+、Cu2+、Na+、C1-、SO42-之间不发生反应,都不与醋酸反应;
B.pH=11的溶液中存大量氢氧根离子,HCO3-与氢氧根离子反应;
C.常温下,
=10-12的溶液中存在大量氢氧根离子,亚铁离子与氢氧根离子反应、次氯酸根离子能够氧化亚铁离子;
D.铁离子能够氧化硫离子、硫离子与铝离子发生双水解反应.
B.pH=11的溶液中存大量氢氧根离子,HCO3-与氢氧根离子反应;
C.常温下,
| c(H+) |
| c(OH-) |
D.铁离子能够氧化硫离子、硫离子与铝离子发生双水解反应.
解答:
解:A.K+、Cu2+、Na+、C1-、SO42-之间不发生反应,且都都不与醋酸反应,在溶液中能够大量共存,故A正确;
B.pH=ll的溶液中存在大量氢氧根离子,HC03-与OH-发生反应,在溶液中不能大量共存,故B错误;
C.此溶液为碱性溶液,OH-与NH4+,OH-与Fe2+不共存,故C错误;
D.Fe3+有氧化性,S2-有还原性,二者发生氧化还原反应,硫离子与铝离子发生双水解反应,在溶液中不能大量共存,故D错误;
故选A.
B.pH=ll的溶液中存在大量氢氧根离子,HC03-与OH-发生反应,在溶液中不能大量共存,故B错误;
C.此溶液为碱性溶液,OH-与NH4+,OH-与Fe2+不共存,故C错误;
D.Fe3+有氧化性,S2-有还原性,二者发生氧化还原反应,硫离子与铝离子发生双水解反应,在溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存,题目难度中等,注意掌握离子反应发生条件,明确常见离子不能共存的情况,如:发生复分解反应、发生氧化还原反应、生成络合物等,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
在一密闭容器中加入一定物质的量的A气体,发生 a A(g)?b B(g)+c C(g)反应,达平衡后,保持温度不变,将容器体积扩大为原来的一倍,当达到新的平衡时c(A)变为原平衡的40%,下列说法正确的是( )
| A、化学计量数之间的关系:a>b+c |
| B、物质B的体积分数减小 |
| C、平衡向正反应方向移动 |
| D、平衡移动过程中,与原平衡相比v正增大、v逆减小 |
下列说法正确的是( )
| A、1molCH4与Cl2发生取代反应最多消耗2molCl2 | ||
| B、乙酸乙酯的水解属于取代反应 | ||
C、CH3-CH═CH2+Cl2
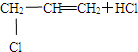 属于加成反应 属于加成反应 | ||
D、甲苯硝化生成三硝基甲苯的化学方程式 |
下列说法正确的是( )
| A、水加热到很高的温度都难分解是因为水分子中存在氢键 |
| B、蔗糖、淀粉、蛋白质及其水解产物均为非电解质 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| D、不用任何试剂即可鉴别Na2CO3溶液和NaHSO4溶液. |
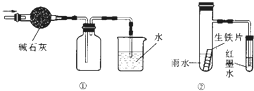
下列有关实验操作或实验原理正确的是( )

| A、提取溴水中的溴,可用加入乙醇萃取的方法 |
| B、用蒸发溶剂的方法将10%的氯化铁溶液变为20%的氯化铁溶液 |
| C、用图 ①的装置可以收集一瓶干燥的氨气 |
| D、用图 ②的装置可以验证生铁片在该雨水中是否会发生吸氧腐蚀 |