题目内容
有机物A(C12H15C1O3)分子为多种官能团芳香族化合物,其结构简式如图1:(其中虚线为未知部分的结构),为推测A的分子结构,进行如图2所示的转化过程(其中部分产物已略):
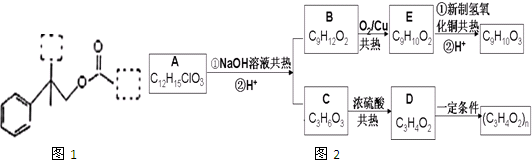
已知D能使溴的CCl4溶液褪色;1mol B最多能与2mol金属钠反应;C催化氧化产物不能发生银镜反应.请回答下列问题:
(1)写出A中官能团的名称: ;C的键线式: .
(2)写出反应类型:C→D ,B→E ;
(3)写出E与新制碱性Cu(OH)2反应的化学方程式 .
(4)E有多种同分异构体,满足下列条件的同分异构体中写出其中任意二种同分异构体的结构简式 .
①含有苯环的一取代结构; ②分子结构中含有甲基; ③能发生水解反应
(5)设计从丙烯合成C的合理路线,用合成路线图的形式表示:(注明必要的反应条件,无机试剂任选)
示例:CH2=CH2
CH3CH2Br
CH3CH2OH.

已知D能使溴的CCl4溶液褪色;1mol B最多能与2mol金属钠反应;C催化氧化产物不能发生银镜反应.请回答下列问题:
(1)写出A中官能团的名称:
(2)写出反应类型:C→D
(3)写出E与新制碱性Cu(OH)2反应的化学方程式
(4)E有多种同分异构体,满足下列条件的同分异构体中写出其中任意二种同分异构体的结构简式
①含有苯环的一取代结构; ②分子结构中含有甲基; ③能发生水解反应
(5)设计从丙烯合成C的合理路线,用合成路线图的形式表示:(注明必要的反应条件,无机试剂任选)
示例:CH2=CH2
| HBr |
| NaOH |
| 水/△ |
考点:有机物的合成
专题:有机物的化学性质及推断
分析:有机物A的分子式为C12H15O3Cl,A在氢氧化钠水溶液发生水解反应、酸化得到B、C,可知A含有酯基,C的催化氧化产物不能发生银镜反应,结合A的部分结构以及B、C分子式可知,A的结构简式为 或
或 ,故C为
,故C为 ,1mol B最多能与2mol金属钠反应,B为
,1mol B最多能与2mol金属钠反应,B为 ,B发生催化氧化生成E为
,B发生催化氧化生成E为 ,E与新制氢氧化铜反应、酸化得到
,E与新制氢氧化铜反应、酸化得到 ,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到
,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到 ,从丙烯合成
,从丙烯合成 ,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、用氢气还原可得
,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、用氢气还原可得 ,据此解答.
,据此解答.
 或
或 ,故C为
,故C为 ,1mol B最多能与2mol金属钠反应,B为
,1mol B最多能与2mol金属钠反应,B为 ,B发生催化氧化生成E为
,B发生催化氧化生成E为 ,E与新制氢氧化铜反应、酸化得到
,E与新制氢氧化铜反应、酸化得到 ,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到
,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到 ,从丙烯合成
,从丙烯合成 ,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、用氢气还原可得
,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、用氢气还原可得 ,据此解答.
,据此解答.解答:
解:有机物A的分子式为C12H15O3Cl,A在氢氧化钠水溶液发生水解反应、酸化得到B、C,可知A含有酯基,C的催化氧化产物不能发生银镜反应,结合A的部分结构以及B、C分子式可知,A的结构简式为 或
或 ,故C为
,故C为 ,1mol B最多能与2mol金属钠反应,B为
,1mol B最多能与2mol金属钠反应,B为 ,B发生催化氧化生成E为
,B发生催化氧化生成E为 ,E与新制氢氧化铜反应、酸化得到
,E与新制氢氧化铜反应、酸化得到 ,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到
,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到 ,
,
(1)A的结构简式为 或
或 ,A中官能团的名称为氯原子、羟基、酯基;C为
,A中官能团的名称为氯原子、羟基、酯基;C为 ,C的键线式为
,C的键线式为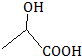 ,
,
故答案为:氯原子、羟基、酯基; ;
;
(2)C→D 是发生消去反应生成碳碳双键,B→E发生醇的催化氧化反应,
故答案为:消去反应;氧化反应;
(3)E与碱性新制Cu(OH)2反应的化学方程式为: +2Cu(OH)2
+2Cu(OH)2
 +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
故答案为: +2Cu(OH)2
+2Cu(OH)2
 +Cu2O↓+2H2O;
+Cu2O↓+2H2O;
(4)E为 ,满足下列条件①含有苯环的一取代结构;②分子结构中含有甲基;③能发生水解反应,说明有酯基,这样的E的同分异构体有
,满足下列条件①含有苯环的一取代结构;②分子结构中含有甲基;③能发生水解反应,说明有酯基,这样的E的同分异构体有 ,
,
故答案为: (其中两种);
(其中两种);
5)从丙烯合成 ,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、再用氢气还原可得
,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、再用氢气还原可得 ,合理的合成路线为CH2=CHCH3
,合理的合成路线为CH2=CHCH3
CH2BrCHBrCH3
CH2OHCHOHCH3
HOOCCOCH3
 ,
,
故答案为:CH2=CHCH3
CH2BrCHBrCH3
CH2OHCHOHCH3
HOOCCOCH3
 .
.
 或
或 ,故C为
,故C为 ,1mol B最多能与2mol金属钠反应,B为
,1mol B最多能与2mol金属钠反应,B为 ,B发生催化氧化生成E为
,B发生催化氧化生成E为 ,E与新制氢氧化铜反应、酸化得到
,E与新制氢氧化铜反应、酸化得到 ,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到
,D能使溴的CCl4溶液褪色,所以C发生消去反应生成D为CH2═CHCOOH,D发生加聚反应得到 ,
,(1)A的结构简式为
 或
或 ,A中官能团的名称为氯原子、羟基、酯基;C为
,A中官能团的名称为氯原子、羟基、酯基;C为 ,C的键线式为
,C的键线式为 ,
,故答案为:氯原子、羟基、酯基;
 ;
;(2)C→D 是发生消去反应生成碳碳双键,B→E发生醇的催化氧化反应,
故答案为:消去反应;氧化反应;
(3)E与碱性新制Cu(OH)2反应的化学方程式为:
 +2Cu(OH)2
+2Cu(OH)2| △ |
 +Cu2O↓+2H2O,
+Cu2O↓+2H2O,故答案为:
 +2Cu(OH)2
+2Cu(OH)2| △ |
 +Cu2O↓+2H2O;
+Cu2O↓+2H2O;(4)E为
 ,满足下列条件①含有苯环的一取代结构;②分子结构中含有甲基;③能发生水解反应,说明有酯基,这样的E的同分异构体有
,满足下列条件①含有苯环的一取代结构;②分子结构中含有甲基;③能发生水解反应,说明有酯基,这样的E的同分异构体有 ,
,故答案为:
 (其中两种);
(其中两种);5)从丙烯合成
 ,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、再用氢气还原可得
,要在丙烯上引入两个官能团,可以先与溴加成,再水解、氧化、再用氢气还原可得 ,合理的合成路线为CH2=CHCH3
,合理的合成路线为CH2=CHCH3| 溴的四氯化碳溶液 |
| 氢氧化钠水溶液 |
| Cu、O2 |
| △ |
| 氢气 |
| 催化剂、△ |
 ,
,故答案为:CH2=CHCH3
| 溴的四氯化碳溶液 |
| 氢氧化钠水溶液 |
| Cu、O2 |
| △ |
| 氢气 |
| 催化剂、△ |
 .
.
点评:本题考查有机物的推断和合成,题目较为综合,难度中等,注意利用A的结构特点与B、C分子式及性质进行推断,是解题关键,需要学生熟练掌握官能团的性质与转化.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
A、5NH4NO3
| ||||
| B、室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | ||||
| C、氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA | ||||
| D、高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA |
将Cl2通入NaOH溶液中,反应得到NaCl,NaClO3,NaClO的混合溶液,其中ClO-、ClO3-的浓度比为1:3,则Cl2与NaOH反应时,被还原的氯元素和被氧化的氯元素的物质的量的比是( )
| A、21:5 | B、11:3 |
| C、3:1 | D、4:1 |
有一包铁粉和铜粉混合物均匀的粉末样品,为了确定其组成,某同学将不同质量的该样品分别与40mL1mol?L-1的FeCl3溶液反应,实验结果如下表所示(忽略反应前后溶液体积的微小变化).
下列实验结论不正确的是( )
| 实验序号 | 一 | 二 | 三 | 四 |
| M(粉末样品)/g | 0.90 | 1.80 | 3.60 | 7.20 |
| M(反应后剩余固体)/g | 0 | 0.64 | 2.48 | 6.08 |
| A、实验一反应后溶液中含有Fe3+、Fe2+、Cu2+ |
| B、实验二、三反应后剩余固体全部是Cu |
| C、实验四的滤液中c(Fe2+)=1.5mol?L-1 |
| D、原粉末样品中m(Fe):m(Cu)=7:8 |
下列各组离子一定能大量共存的是( )
| A、醋酸溶液中:K+、Cu2+、Na+、C1-、SO42- | ||
| B、pH=ll的溶液中:HCO3-、Na+、NH3.H2O、NO3- | ||
C、常温下,
| ||
| D、在含有大量Fe3+的溶液中:A13+、Na+、S2-、Br- |
下列装置或操作能达到实验目的是( )
A、 除去CO2中的HCl |
B、 稀释浓硫酸 |
C、 检查装置气密性 |
D、 实验室制备乙烯 实验室制备乙烯 |
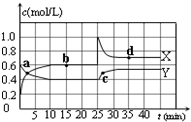 已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示. 某有机物M的球棍模型如图所示:
某有机物M的球棍模型如图所示:
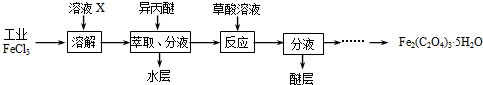
 三氯化铁是合成草酸铁的重要原料.
三氯化铁是合成草酸铁的重要原料.