题目内容
8.下列除杂质的操作中不正确的是( )| A. | Na2CO3 固体中混有少量NaHCO3:加热固体至质量恒定 | |
| B. | NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体 | |
| C. | CO2中混有HCl:将其通过装NaOH溶液的洗气瓶 | |
| D. | NaCl溶液中混有少量I2:加入适量CCl4,振荡,静置,分液 |
分析 A.NaHCO3不稳定,解热可分解生成Na2CO3;
B.溶液中Na2CO3能与CO2、H2O反应生成NaHCO3;
C.二者都可与氢氧化钠溶液反应;
D.碘易溶于四氯化碳.
解答 解:A.NaHCO3不稳定,解热可分解生成Na2CO3,可用于除杂,故A正确;
B.向Na2CO3中通入二氧化碳,会反应生成碳酸氢钠溶液,达到除杂的目的,故B正确;
C.二者都可与氢氧化钠溶液反应,应用饱和碳酸氢钠溶液,故C错误;
D.碘易溶于四氯化碳,可用萃取的方法除杂,故D正确.
故选C.
点评 本题考查物质的分离、提纯及除杂,为高频考点,把握物质的性质及混合物分离提纯方法为解答的关键,注重基础知识的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
19.如图所示实验装置进行相应实验,能达到实目的是( )
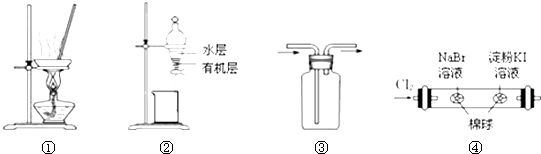

| A. | 用图①所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体 | |
| B. | 用图②所示装置,分离CCl4萃取碘水后的有机层和水层 | |
| C. | 按装置③所示的气流方向可用于收集H2、NH3等 | |
| D. | 用图④所示装置,可以证明氧化性:Cl2>Br2>I2 |
16. 已知室温下,某些弱酸的电离常数如下:
已知室温下,某些弱酸的电离常数如下:
(1)常温下,物质的量浓度相同的下列四种溶液:
a.盐酸溶液 b.硫酸溶液 c.次氯酸溶液 d.醋酸溶液
①H+由大到小的顺序是:b、a、d、c(填字母)
②等体积a、b、d三种溶液与足量的锌完全反应,在相同的条件下,生成氢气的体积关系为b>a=d或b=2a=2d(用字母及“>”“<”“=”表示)
③欲降低稀硫酸与足量锌生成氢气速率,但不影响产生氢气的物质的量,下列措施可行的是abd
a.加水稀释 b.加入Na2SO4溶液 c.加入Na2CO3固体 d.加入CH3COONa固体
(2)某温度下pH均为4的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化如图所示,其中表示醋酸的曲线是b,该醋酸溶液稀释过程中,下列各量一定变小的是AC
A.c(H+) B.$\frac{c(C{H}_{3}COOH).c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$ C.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$
(3)新制饱和氯水中存在Cl2+H2O?HCl+HClO,为使HClO浓度增大,下列措施可行的B
A.加少量NaOH固体 B.加CaCO3固体 C.加NaCl固体.
 已知室温下,某些弱酸的电离常数如下:
已知室温下,某些弱酸的电离常数如下:| CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | 1.7×10-5 | Ka1=4.2.×10-7 Ka2=5.6.×10-11 | 3×10-8 |
a.盐酸溶液 b.硫酸溶液 c.次氯酸溶液 d.醋酸溶液
①H+由大到小的顺序是:b、a、d、c(填字母)
②等体积a、b、d三种溶液与足量的锌完全反应,在相同的条件下,生成氢气的体积关系为b>a=d或b=2a=2d(用字母及“>”“<”“=”表示)
③欲降低稀硫酸与足量锌生成氢气速率,但不影响产生氢气的物质的量,下列措施可行的是abd
a.加水稀释 b.加入Na2SO4溶液 c.加入Na2CO3固体 d.加入CH3COONa固体
(2)某温度下pH均为4的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化如图所示,其中表示醋酸的曲线是b,该醋酸溶液稀释过程中,下列各量一定变小的是AC
A.c(H+) B.$\frac{c(C{H}_{3}COOH).c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$ C.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$
(3)新制饱和氯水中存在Cl2+H2O?HCl+HClO,为使HClO浓度增大,下列措施可行的B
A.加少量NaOH固体 B.加CaCO3固体 C.加NaCl固体.
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,16gCH4含有10NA个电子 | |
| B. | 0.1mol•L-1的盐酸溶液中含有0.1NA个H+ | |
| C. | 1molNa与乙醇完全反应,失去2NA个电子 | |
| D. | 标准状况下,22.4L苯含有NA个苯分子 |
13.将过量的铁粉投入到盛有硫酸铜和稀硫酸的混合溶液中,充分反应后,过滤,滤液中含有物质是( )
| A. | 硫酸铁 | B. | 硫酸铜 | C. | 硫酸 | D. | 硫酸亚铁 |
20.CCUS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化,产生经济效益.
(1)已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1=-820kJ/mol
CO(g)+H2O(g)═CO2(g)+H2(g)△H2=-41.2kJ/mol
2CO(g)+O2(g)═2CO2(g)△H3=-566kJ/mol则反应的
CO2(g)+CH4(g)═2CO(g)+2H2(g)△H=+229.6kJ/mol
(2)工业上,可利用太阳能以CO2为原料制取C,其原理如图1所示:整个过程中FeO(填“Fe3O4”或“FeO”)是反应的催化剂.重整系统中发生的反应为:6FeO+CO2$\frac{\underline{\;700K\;}}{\;}$2Fe3O4+C每生成1mol Fe3O4,转移电子的物质的量为2mol.
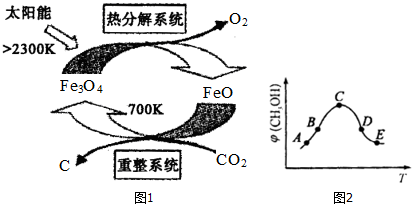
(3)CO2还可用于合成甲醇,反应方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0
①该反应的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.
②在恒容的密闭容器中,加入H2和CO2的混合气体,不同温度条件,反应相同时间后,测得甲醇的体积分数(CH3OH)如图2所示.图中A、B、C、D、E五个点对应的状态中,处于平衡状态的是C、D、E(填字母),B点和E点的反应速率大小关系为v(B)<v(E)(填“>”、“<”、“=”).
③一定温度下,在甲、乙两个容积相同的恒容密闭容器中,加入H2和CO2的混合气体.
甲容器平衡后气体的压强为开始时的80%,要使乙容器达平衡时与甲容器达到相同的平衡状态,且起始时反应逆向进行,则c的取值范围为0.4<n(c)≤1mol.
(1)已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1=-820kJ/mol
CO(g)+H2O(g)═CO2(g)+H2(g)△H2=-41.2kJ/mol
2CO(g)+O2(g)═2CO2(g)△H3=-566kJ/mol则反应的
CO2(g)+CH4(g)═2CO(g)+2H2(g)△H=+229.6kJ/mol
(2)工业上,可利用太阳能以CO2为原料制取C,其原理如图1所示:整个过程中FeO(填“Fe3O4”或“FeO”)是反应的催化剂.重整系统中发生的反应为:6FeO+CO2$\frac{\underline{\;700K\;}}{\;}$2Fe3O4+C每生成1mol Fe3O4,转移电子的物质的量为2mol.

(3)CO2还可用于合成甲醇,反应方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0
①该反应的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.
②在恒容的密闭容器中,加入H2和CO2的混合气体,不同温度条件,反应相同时间后,测得甲醇的体积分数(CH3OH)如图2所示.图中A、B、C、D、E五个点对应的状态中,处于平衡状态的是C、D、E(填字母),B点和E点的反应速率大小关系为v(B)<v(E)(填“>”、“<”、“=”).
③一定温度下,在甲、乙两个容积相同的恒容密闭容器中,加入H2和CO2的混合气体.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、c molCH3OH(g)、c molH2O(g) |
17.A、B、C、D是四种短周期元素,它们的原子序数依次增大.其中A、D元素同主族,B、C元素同周期;由A、B、C、D中的两种元素可形成原子个数比为1:1的多种化合物,甲、乙、丙、丁为其中的四种,它们的元素组成如下表所示:
常温下,甲物质为气体,密度略小于空气;乙物质为液体;丙物质和丁物质为固体且都为离子化合物.请填写下列空白:
(1)丙物质的化学式为NaH,丁物质中阴离子与阳离子的个数之比为1:2.
(2)研究表明乙物质具有弱酸性,则乙物质在水中的电离方程式为H2O2?H++HO2-.
(3)某同学设计了一个以结构简式为 BA3-CA的物质为燃料的电池,并用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如图1:
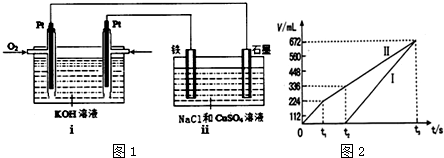
①写出ⅰ中通入该物质这一极的电极反应式CH3OH-6e-+8OH-=CO32-+6H2O.
②理论上ⅱ中两极所得气体的体积随时间变化的关系如坐标图2所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式2 H2O-4e-=O2↑+4 H+;;原混合液中CuSO4溶液物质的量浓度为0.1 mol/L.
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 组成元素 | B、C | A、C | A、D | C、D |
(1)丙物质的化学式为NaH,丁物质中阴离子与阳离子的个数之比为1:2.
(2)研究表明乙物质具有弱酸性,则乙物质在水中的电离方程式为H2O2?H++HO2-.
(3)某同学设计了一个以结构简式为 BA3-CA的物质为燃料的电池,并用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如图1:

①写出ⅰ中通入该物质这一极的电极反应式CH3OH-6e-+8OH-=CO32-+6H2O.
②理论上ⅱ中两极所得气体的体积随时间变化的关系如坐标图2所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式2 H2O-4e-=O2↑+4 H+;;原混合液中CuSO4溶液物质的量浓度为0.1 mol/L.
18.下列关系不正确的是( )
| A. | 非金属性:N>P>As>Sb>Bi | B. | 酸性:HNO3>H3PO4>H3AsO4>H3SbO4 | ||
| C. | 稳定性:NH3<PH3<AsH3<SbH3 | D. | 稳定性:HCl>H2S>PH3>SiH4 |
