题目内容
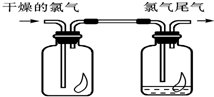 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用 氢氧化钠(NaOH)溶液吸收多余的氯
气,原理是
石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
A.O2 B.Cl2 C.CO2 D.HClO
(3)当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCl C.KBr D.Na2CO3
(4)实验室中常用来制备氯气的化学方程式为
考点:探究氯水、氯气的漂白作用
专题:卤族元素
分析:(1)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性;
(2)利用氯气和氢氧化钠溶液反应来处理尾气,漂白粉的有效成分是次氯酸钙,长期露置于空气中的漂白粉,变质生成碳酸钙,加稀盐酸后产生的气体为二氧化碳;
(3)依据氯气的物理性质和化学性质的应用分析判断;
(4)实验室中用二氧化锰和浓盐酸加热来制取氯气.
(2)利用氯气和氢氧化钠溶液反应来处理尾气,漂白粉的有效成分是次氯酸钙,长期露置于空气中的漂白粉,变质生成碳酸钙,加稀盐酸后产生的气体为二氧化碳;
(3)依据氯气的物理性质和化学性质的应用分析判断;
(4)实验室中用二氧化锰和浓盐酸加热来制取氯气.
解答:
解:(1)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性;Cl2+H2O=HCl+HClO;干燥的有色布条无明显现象,潮湿的有色布条褪色,
故答案为:干燥的有色布条无明显现象,潮湿的有色布条褪色;
(2)为了防止氯气尾气污染空气,可用NaOH溶液吸收,该反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,工业上常用廉价的石灰乳吸 收工业氯气尾气制得漂白粉,漂白粉的有效成分是次氯酸钙Ca(ClO)2;长期露置于空气中的漂白粉,会和空气中的二氧化碳水反应生成碳酸钙和次氯酸,次氯酸分解,最后组要是碳酸钙,加稀盐酸后产生的气体是二氧化碳;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;Ca(ClO)2;C;
(3)当氯气泄漏人们逃离现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,水溶液能较易吸收氯气,但不能对人有腐蚀作用;
A、NaOH是强碱具有强腐蚀性,故不选;
B、NaCl 不能吸收氯气,故不选;
C、KBr不能吸收氯气,故不选;
D、Na2CO3溶液水解显碱性,可以吸收氯气,腐蚀性较小,符合要求,故可选;
故答案为:D
(4)实验室中用二氧化锰和浓盐酸加热来制取氯气,原理是:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O.
故答案为:干燥的有色布条无明显现象,潮湿的有色布条褪色;
(2)为了防止氯气尾气污染空气,可用NaOH溶液吸收,该反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,工业上常用廉价的石灰乳吸 收工业氯气尾气制得漂白粉,漂白粉的有效成分是次氯酸钙Ca(ClO)2;长期露置于空气中的漂白粉,会和空气中的二氧化碳水反应生成碳酸钙和次氯酸,次氯酸分解,最后组要是碳酸钙,加稀盐酸后产生的气体是二氧化碳;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;Ca(ClO)2;C;
(3)当氯气泄漏人们逃离现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,水溶液能较易吸收氯气,但不能对人有腐蚀作用;
A、NaOH是强碱具有强腐蚀性,故不选;
B、NaCl 不能吸收氯气,故不选;
C、KBr不能吸收氯气,故不选;
D、Na2CO3溶液水解显碱性,可以吸收氯气,腐蚀性较小,符合要求,故可选;
故答案为:D
(4)实验室中用二氧化锰和浓盐酸加热来制取氯气,原理是:MnO2+4HCl(浓)
| ||
故答案为:MnO2+4HCl(浓)
| ||
点评:本题考查了氯气及其化合物性质的应用,主要考查氯气与水反应生成的次氯酸的强氧化性、漂白性的应用,气体吸收方法,较简单.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
某溶液可能含有Cl-、SO42-、CO32-、OH-、NH4+、Al3+、Fe3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6g固体;向上述滤液中加足量BaCl2溶液,得到 6.99g不溶于盐酸的沉淀.下列关于原溶液的说法正确的是( )
| A、原溶液中至少存在3种离子 |
| B、原溶液中一定不存在的离子是:Cl-、CO32-、OH- |
| C、原溶液中可能存在的离子有:Cl-、Al3+和K+ |
| D、原溶液中一定存在的离子是:NH4+、Fe3+、SO42-和Cl-,且c(Cl-)≥0.2mol/L |
有关烷烃的叙述:①都是易燃物②特征反应是取代反应③碳原子数相邻的两个烷烃分子在组成上相差一个“-CH3”,其中正确的是( )
| A、①② | B、①③ | C、① | D、②③ |
常温下,下列有关物质的量浓度关系正确的是( )
| A、等物质的量浓度的溶液中,水电离出的c(H+):HCl>CH3COOH |
| B、pH相同的溶液中:c(Na2CO3)<c(NaHCO3) |
| C、在Na2SO3溶液中:c(Na+)=2c(SO32-)+c(HSO3-)+c(OH-) |
| D、0.1mol?L-1 NaHS溶液中:c(Na+)=c(HS-) |
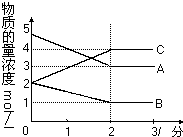 在密闭容器中,某反应在不同反应时间各物质的量的变化情况如右图所示(各物质均为气体).
在密闭容器中,某反应在不同反应时间各物质的量的变化情况如右图所示(各物质均为气体). 碱式碳酸铝镁[MgaAlb(OH)c(CO3)d?xH2O]常用作塑料阻燃剂.
碱式碳酸铝镁[MgaAlb(OH)c(CO3)d?xH2O]常用作塑料阻燃剂.