题目内容
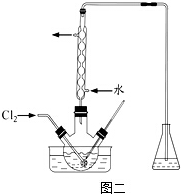
某研究性学习小组为研究氯气是否具有漂白性,设计如下实验装置.试根据实验装置回答下列问题:

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液
(1)在常温下,KMnO4固体粉末可以与浓盐酸反应生成氯气,其反应方程式为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的 .
(2)B中的液体为 .
(3)D中NaOH溶液的作用 .
(4)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去.组内有甲、乙两种意见:
甲:氯气溶于水溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色.
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则 的意见正确.(填“甲”或“乙”)

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液
(1)在常温下,KMnO4固体粉末可以与浓盐酸反应生成氯气,其反应方程式为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的
(2)B中的液体为
(3)D中NaOH溶液的作用
(4)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去.组内有甲、乙两种意见:
甲:氯气溶于水溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色.
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则
考点:探究氯水、氯气的漂白作用
专题:卤族元素
分析:(1)高锰酸钾固体和浓盐酸反应制备氯气,反应不需要加热,为固体与液体反应,据此结合图象判断;
(2)浓硫酸具有吸水性,能吸收氯气中的水蒸气;
(3)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,可吸收多余的氯气;
(4)继续滴加碱,若红色恢复说明酸碱中和使碱减少,若红色不恢复,则说明是次氯酸的作用.
(2)浓硫酸具有吸水性,能吸收氯气中的水蒸气;
(3)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,可吸收多余的氯气;
(4)继续滴加碱,若红色恢复说明酸碱中和使碱减少,若红色不恢复,则说明是次氯酸的作用.
解答:
解:(1)高锰酸钾固体和浓盐酸反应制备氯气,反应不需要加热,为固体与液体反应,且氯气能溶于水,甲装置适用于固体和液体加热制备气体,乙装置适用于固体和液体反应,要求固体难溶于水且生成的气体难溶于水,丙装置适合,故选丙,
故答案为:丙;
(2)浓硫酸具有吸水性,且浓硫酸和氯气不反应,所以浓硫酸的作用是干燥氯气,
故答案为:浓硫酸;
(3)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,反应离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:吸收多余的氯气;
(4)因在褪色后的溶液中逐渐加入足量的NaOH溶液,因溶液中有酚酞,碱性溶液应显红色,溶液一直未见红色,说明氯气溶于水生成漂白性物质,使溶液褪为无色,不是由于碱被中和褪色,故乙正确,
故答案为:乙.
故答案为:丙;
(2)浓硫酸具有吸水性,且浓硫酸和氯气不反应,所以浓硫酸的作用是干燥氯气,
故答案为:浓硫酸;
(3)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,反应离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:吸收多余的氯气;
(4)因在褪色后的溶液中逐渐加入足量的NaOH溶液,因溶液中有酚酞,碱性溶液应显红色,溶液一直未见红色,说明氯气溶于水生成漂白性物质,使溶液褪为无色,不是由于碱被中和褪色,故乙正确,
故答案为:乙.
点评:本题考查氯气的性质与实验室制备,掌握氯气实验室制备的原理与注意事项以及氯水的漂白原理是解答本题的关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法中,正确的是( )
| A、将NO2通入FeSO4溶液中不会有明显现象 |
| B、2L 0.5mol/L的盐酸和1L 0.5mol/L的硫酸PH相等 |
| C、饱和氯水中:c(H+)>c(Cl-)>c(HClO)>c(ClO-) |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下反应的△H不相同 |
下列性质比较中,正确的是( )
| A、热稳定性:CH4>SiH4 |
| B、酸性:H2SO4>HClO4 |
| C、熔点、沸点:O2>S |
| D、原子半径:N>P |
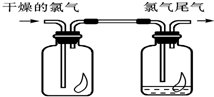 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是

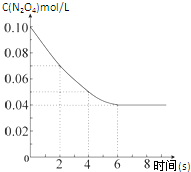 在温度为298K时,将0.10mol无色的N2O4气体放入1L抽空的密闭容器中,出现红棕色,直至建立N2O4(g)?2NO2(g)的平衡.下图表示测定N2O4的浓度与时间关系的曲线(纵坐标为N2O4的浓度,横坐标为时间).
在温度为298K时,将0.10mol无色的N2O4气体放入1L抽空的密闭容器中,出现红棕色,直至建立N2O4(g)?2NO2(g)的平衡.下图表示测定N2O4的浓度与时间关系的曲线(纵坐标为N2O4的浓度,横坐标为时间).