题目内容
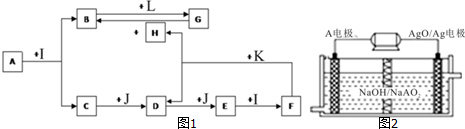
2.工业生产硝酸铵的流程如图1所示
(1)硝酸铵的水溶液呈酸性(填“酸性”、“中性”或“碱性”);其水溶液中各离子的浓度大小顺序为:c(NO3-)>c(NH4+)>c(H+)>c(OH-).
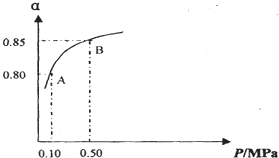
(2)已知N2(g)+3H2(g)?2NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如2图.
①曲线a对应的温度是200℃.
②关于工业合成氨的反应,下列叙述正确的是ACE
A.及时分离出NH3可以提高H2的平衡转化率
B.P点原料气的平衡转化率接近100%,是当前工业生产工艺中采用的温度、压强条件
C.图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
D.M点比N点的反应速率快
E.如果N点时c(NH3)=0.2mol•L-1,N点的化学平衡常数K≈0.93
(3)尿素(H2NCONH2)是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为二步反应:
第一步:2NH3(g)+CO2(g)═H2NCOONH4(s)△H=-272kJ•mol-1
第二步:H2NCOONH4(s)═CO(NH2)2(s)+H2O(g)△H=+138kJ•mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式:2NH3(g)+CO2(g)?H2O(g)+CO(NH2)2 (s)△H=-134kJ/mol;
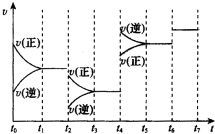
(4)某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如图3所示:
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第二步反应决定,总反应进行到55min时到达平衡.
②在图4中画出第二步反应的平衡常数K随温度的变化的示意图.
分析 (1)硝酸铵溶液中铵根离子水解,使溶液呈酸性;
(2)①正反应是放热反应,升高温度平衡逆向移动,氨气的含量减小;
②A.减小生成物浓度平衡正向移动;
B.P点原料气的平衡转化率接近100%,但此时压强为100MPa,高压对设备的要求太高,导致成本高,不是当前工业生产工艺中采用的温度、压强条件;
C.K只受温度影响,温度不变平衡常数不变,正反应为放热反应,升高温度平衡逆向移动,平衡常数减小;
D.温度越高反应速率越快;
E.计算平衡时各组分浓度,代入K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$计算平衡常数;
(3)已知:①2NH3(g)+CO2(g)═H2NCOONH4(s)△H=-272kJ•mol-1;
②H2NCOONH4(s)═CO(NH2)2(s)+H2O(g)△H=+138kJ•mol-1;
根据盖斯定律,①+②可得:2NH3(g)+CO2(g) H2O(g)+CO(NH2)2 (s);
H2O(g)+CO(NH2)2 (s);
(4)①已知总反应的快慢由慢的一步决定,反应快慢可以依据第一步和第二步反应的曲线斜率比较大小;
②第二步反应为吸热反应,升高温度平衡向正反应方向移动,平衡常数增大.
解答 解:(1)硝酸铵溶液中铵根离子水解,会使溶液呈酸性,所以溶液中离子浓度大小关系是c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:酸性;c(NO3-)>c(NH4+)>c(H+)>c(OH-);
(2)①合成氨的反应为放热反应,反应温度越高,越不利于反应正向进行,曲线a的氨气的物质的量分数最高,其反应温度对应相对最低,所以a曲线对应温度为200°C;
故答案为:200℃;
②A.及时分离出NH3,可以使平衡正向进行,可以提高H2的平衡转化率,故A正确;
B.P点原料气的平衡转化率接近100%,但此时压强为100MPa,高压对设备的要求太高,导致成本高,当前工业生产工艺中采用的500℃、20MPa~50MPa,故B错误;
C.平衡常数与温度有关,与其他条件无关,温度相同时平衡常数相同,反应是放热反应,温度越高平衡常数越小,则M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N),故C正确;
D.N点温度高于M点,温度越低反应速率越快,故N点比M点的反应速率快,故D错误;
E.N点时c(NH3)=0.2mol•L-1,氨气体积分数为20%,则:
N2(g)+3H2(g)?2NH3(g)
起始浓度(mol/L):x 3x 0
变化浓度(mol/L):0.1 0.3 0.2
平衡浓度(mol/L):x-0.1 3x-0.3 0.2
所以$\frac{0.2}{4x-0.2}$=20%,解得x=0.3,平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$=$\frac{0.{2}^{2}}{0.2×0.{6}^{3}}$≈0.93,故E正确,
故选:ACE;
(3)已知:①2NH3(g)+CO2(g)═H2NCOONH4(s)△H=-272kJ•mol-1;
②H2NCOONH4(s)═CO(NH2)2(s)+H2O(g)△H=+138kJ•mol-1;
根据盖斯定律,①+②可得:2NH3(g)+CO2(g)?H2O(g)+CO(NH2)2 (s)△H=-134kJ/mol,
故答案为:2NH3(g)+CO2(g)?H2O(g)+CO(NH2)2 (s)△H=-134kJ/mol;
(4)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二步反应,从曲线斜率不难看出第二步反应速率慢,所以合成尿素总反应的快慢由第二步反应决定,根据图可知,尿素在55分钟时,物质的量不再变化,即反应达到平衡,所以总反应进行到55min时到达平衡,
故答案为:二;55;
②第二步反应为吸热反应,升高温度平衡向正反应方向移动,平衡常数增大,所以第二步反应的平衡常数K随温度的变化的示意图为 ,故答案为:
,故答案为: .
.
点评 本题考查化学平衡计算与影响因素、化学平衡图象、热化学方程式的书写、盐类水解等,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学计算能力,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 明矾净化水 | B. | 纯碱除去油污 | ||
| C. | 臭氧用于餐具消毒 | D. | 食醋清洗水垢 |
(1)久置的绿矾溶液容易被空气氧化变质,简述检验绿矾溶液已经变质的操作和现象:取少量待测液于试管中,向其中滴入2~3滴的KSCN溶液,震荡,溶液变成红色.
(2)绿矾溶液浓度的标定测定溶液中Fe2+物质的量浓度的方法是:a.量取25.00mL待测溶液于锥形瓶中;b.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点;c.重复操作2次,消耗KMnO4溶液体积的体积分别为20.02mL、24.98mL、19.98mL.
(已知滴定时发生反应的离子方程式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)
计算上述滤液中Fe2+物质的量浓度0.04000 mol/L(保留四位有效数字).
(3)探究保存绿矾溶液的有效措施
【反应原理】Fe2+在空气中易氧化变质,完成并配平下列离子方程式:
12Fe2++3O2+6H2O=4Fe(OH)3↓+8Fe3+
【操作现象】取4支试管,如图进行实验,请写出试管①的现象和加入④的试剂.
 |  |  |  | |
| 添加试剂 | 10.0mlFeSO4溶液 | 10.0mlFeSO4溶液+2ml煤油 | 10.0mlFeSO4溶液+1.0铁粉 | 10.0mlFeSO4溶液+ 少量(或几滴)硫酸 |
| 3天内的现象 | 溶液颜色很快变成黄色,并出现棕黄色浑浊 | / | / | / |
| A. | NH4HSO3溶液与足量NaOH溶液共热:NH4++HSO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+SO32-+2H2O | |
| B. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 用盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2 MnO4-+6H++5H2O2═2Mn2++5 O2↑+8H2O | |
| D. | 用石墨电极电解饱和MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH- |
| A. | Na2CO3溶液的碱性增强 | |
| B. | 阳极反应:CO32--2e-+H2O═CO2↑+2OH- | |
| C. | 溶液中CO32-+H2O?HCO3-+OH-平衡不移动 | |
| D. | 向溶液中加入一定量HCOOH的能复原 |
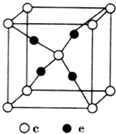 周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题: .
.