题目内容
13.在1200℃时,天然气脱硫工艺中会发生下列反应H2S(g)+$\frac{3}{2}$O2(g)=SO2(g)+H2O(g)△H1
2H2S(g)+SO2(g)=S2(g)+2H2O (g)△H2
H2S(g)+O2(g)=S(g)+H2O(g)△H3
2S(g)=S2(g)△H4
则△H4的正确表达式为( )
| A. | △H4=$\frac{3}{2}$(△H1+△H2+3△H3) | B. | △H4=$\frac{2}{3}$(3△H3-△H1-△H2) | ||
| C. | △H4=$\frac{2}{3}$ (△H1+△H2-3△H3) | D. | △H4=$\frac{3}{2}$(△H1-△H2-3△H3) |
分析 由①H2S(g)+$\frac{3}{2}$O2(g)=SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)=S2(g)+2H2O (g)△H2
③H2S(g)+O2(g)=S(g)+H2O(g)△H3
结合盖斯定律可知,(①+②-③×3)×$\frac{2}{3}$得到2S(g)=S2,以此来解答.
解答 解:由①H2S(g)+$\frac{3}{2}$O2(g)=SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)=S2(g)+2H2O (g)△H2
③H2S(g)+O2(g)=S(g)+H2O(g)△H3
结合盖斯定律可知,(①+②-③×3)×$\frac{2}{3}$得到2S(g)=S2,
则2S(g)=S2(g)△H4=$\frac{2}{3}$ (△H1+△H2-3△H3),
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应的关系、盖斯定律的应用为解答的关键,侧重分析与应用能力的考查,注意已知反应与目标反应的关系,题目难度不大.

练习册系列答案
相关题目
10.与OHCCH2CH2CHO互为同系物且相对分子质量比其大28的同分异构体有( )
| A. | 5种 | B. | 7种 | C. | 9种 | D. | 11种 |
1.以粗氧化锌粉(含FeO、Fe2O3、ZnS等)制取活性ZnO的工艺如下:
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品.
已知:离子沉淀的pH见下表.
(1)加入H2O2时能浸出硫化锌,同时生成淡黄色固体,写出其化学方程式ZnS+H2O2+H2SO4=ZnSO4+2H2O+S.
(2)步骤2中调节溶液pH的范围是3.7~5.4.
(3)取洗涤、干燥后的碱式碳酸锌68.2g,充分灼烧后测得残留物质的质量为48.6g,将所得气体通入足量澄清石灰水中,得沉淀20g.计算碱式碳酸锌的组成(用化学式表示,写出计算过程).ZnCO3•2Zn(OH)2•H2O 或Zn3(OH)4CO3•H2O.
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品.
已知:离子沉淀的pH见下表.
| 离子 | 开始沉淀pH | 沉淀完全pH |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Zn2+ | 5.4 | 8.0 |
(2)步骤2中调节溶液pH的范围是3.7~5.4.
(3)取洗涤、干燥后的碱式碳酸锌68.2g,充分灼烧后测得残留物质的质量为48.6g,将所得气体通入足量澄清石灰水中,得沉淀20g.计算碱式碳酸锌的组成(用化学式表示,写出计算过程).ZnCO3•2Zn(OH)2•H2O 或Zn3(OH)4CO3•H2O.
8.下列说法正确的是( )
| A. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| B. | 在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是Cu | |
| C. | 能与酸反应生成盐和水的氧化物一定是碱性氧化物 | |
| D. | 将Ba(OH)2溶液滴到明矾溶液中,当SO42-刚沉淀完时,铝以AlO2-的形式存在 |
18.下列有关物质性质的比较,错误的是( )
| A. | 溶解度:小苏打<苏打 | B. | 沸点:K>Na | ||
| C. | 密度:溴>水 | D. | 热稳定性:HF>HCl |
2.下列表示对应化学反应的离子方程式正确的是( )
| A. | 氢氧化铁溶于氢碘酸溶液中:Fe(OH)3+3HI═Fe3++3I-+3H2O | |
| B. | 少量CO2通入苯酚钠溶液中: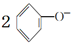 +H2O+CO2→ +H2O+CO2→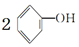 +CO32- +CO32- | |
| C. | 向NaAlO2溶液中通入足量CO2:2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| D. | Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |