题目内容
10.关于二氧化硫和二氧化氮叙述正确的是( )| A. | 两种气体都是无色有毒的气体,且都可用水吸收以消除对空气的污染 | |
| B. | 二氧化硫与过量的二氧化氮混合后通入水中能得到两种常用的强酸 | |
| C. | 两种气体都具有强氧化性,因此都能够使品红溶液褪色 | |
| D. | 两种气体溶于水都可以与水反应,且只生成相应的酸 |
分析 A、二氧化氮是红棕色气体,与水反应生成有毒的气体;
B、二氧化硫与过量的二氧化氮混合后通入水中发生氧化还原反应,能得到硫酸和硝酸;
C、二氧化硫使品红褪色非氧化还原;
D、二氧化硫溶于水生成亚硫酸相应的酸,二氧化氮生成硝酸.
解答 解:A、二氧化氮是红棕色气体,与水反应生成有毒的一氧化氮气体,故A错误;
B、二氧化硫与过量的二氧化氮混合后通入水中发生氧化还原反应,能得到硫酸和硝酸,两种强酸,故B正确;
C、二氧化硫使品红褪色非氧化还原,形成无色不稳定的大分子,故C错误;
D、二氧化硫溶于水生成亚硫酸相应的酸,二氧化氮生成硝酸,不是相应的酸,故D错误;
故选B.
点评 本题考查二氧化硫和二氧化氮性质的比较,两种气体都有毒,二氧化氮是红棕色的气体,学生只要掌握基础就可以解题,比较容易.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
20.下列反应既属于氧化还原反应,又是吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 水分解生成氢气和氧气 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
1.已知某元素M原子的最外层电子排布式为nS1,下列说法正确的是( )
| A. | M一定是金属元素 | B. | M一定是S区元素 | C. | M的最高价是+1价 | D. | M可能呈现出-1价 |
18.X、Y、Z、W、R、P、Q是短周期主族元素,部分信息如表所示:
(1)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为同位素.
(2)Z的单质与水反应的化学方程式是2Na+2H2O=2NaOH+H2↑;R与Q两元素最高价氧化物水化物反应的离子方程式3H++Al(OH)3═Al3++3H2O.
(3)Y与R相比,非金属性较强的是Cl(用元素符号表示),下列事实能证明这一结论的是bc(填字母序号).
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)写出工业制取Y的单质的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(5)反应3X2(g)+P2(g) 2PX3(g)过程中的能量变化如图所示,回答下列问题.
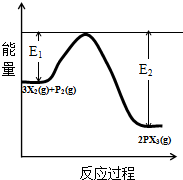
①该反应是放热反应(填“吸热”“放热”);
②反应体系中加入催化剂对反应热是否有影响?不影响,原因是催化剂不改变平衡的移动(从能量说明)
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -3,+5 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Z的单质与水反应的化学方程式是2Na+2H2O=2NaOH+H2↑;R与Q两元素最高价氧化物水化物反应的离子方程式3H++Al(OH)3═Al3++3H2O.
(3)Y与R相比,非金属性较强的是Cl(用元素符号表示),下列事实能证明这一结论的是bc(填字母序号).
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)写出工业制取Y的单质的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(5)反应3X2(g)+P2(g) 2PX3(g)过程中的能量变化如图所示,回答下列问题.

①该反应是放热反应(填“吸热”“放热”);
②反应体系中加入催化剂对反应热是否有影响?不影响,原因是催化剂不改变平衡的移动(从能量说明)
19.某合金由铜、镁两种金属组成,现取合金5.0g于烧杯中,将100g稀盐酸分两次加人到烧杯中,所得数据如下表.
请计算:
(1)合金中镁的质量为4g;
(2)所用稀盐酸的溶质质量分数.
| 次数 | 第1次 | 第2次 |
| 加入稀盐酸的质量/g | 50 | 50 |
| 剩余固体的质量/g | 2.6 | 1 |
(1)合金中镁的质量为4g;
(2)所用稀盐酸的溶质质量分数.
1.一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )


| A. | 反应CH4+H2O $\frac{\underline{催化剂}}{△}$3H2+CO,每消耗1 mol CH4转移12 mol电子 | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-═2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 电极B上发生的电极反应为:O2+2CO2+4e-═2CO32- |
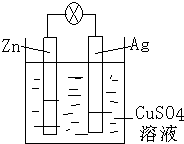 如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液,回答下列问题:
如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液,回答下列问题: