题目内容
2.1mol某有机物在与3mol氧气恰好完全反应,生成2molCO2和3molH2O,通过计算确定该有机物中是(填“是”或“否”)含有氧;求该有机物的分子式.分析 根据原子守恒判断有机物是否含有元素,计算确定有机物分子式.
解答 解:1mol某有机物在与3mol氧气恰好完全反应,生成2molCO2和3molH2O,
生成物中O原子物质的量为2mol×2+3mol=7mol,而3mol氧气中含有氧原子为3mol×2=6mol<7mol,故有机物含有氧元素,
1mol有机物含有氧原子为7mol-6mol=1mol,含有碳原子为2mol,含有H原子为3mol×2=6mol,故有机物分子式为C2H6O,
故答案为:是;C2H6O.
点评 本题考查有机物分子式确定,掌握燃烧法利用原子守恒确定有机物分子式,有利于基础知识的巩固.

练习册系列答案
相关题目
12.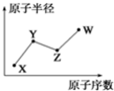 W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1,下列说法正确的是( )
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1,下列说法正确的是( )
 W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1,下列说法正确的是( )
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1,下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | X、Y、Z三种元素形成的化合物均为强酸 | |
| C. | Y的氢化物可用于检验W的单质是否泄漏 | |
| D. | 如W的单质泄漏,可以用湿毛巾蘸Y的氢化物的水溶液逃生 |
13.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾与水反应生成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 当光束通过鸡蛋清水溶液时,能观察到丁达尔效应 | |
| C. | Li是最轻的金属,也是活动性较强的金属,是制造电池的理想物质 | |
| D. | 水泥厂用高压电作用于气溶胶以除去烟尘,是根据胶体带电这个性质而设计的 |
10.关于二氧化硫和二氧化氮叙述正确的是( )
| A. | 两种气体都是无色有毒的气体,且都可用水吸收以消除对空气的污染 | |
| B. | 二氧化硫与过量的二氧化氮混合后通入水中能得到两种常用的强酸 | |
| C. | 两种气体都具有强氧化性,因此都能够使品红溶液褪色 | |
| D. | 两种气体溶于水都可以与水反应,且只生成相应的酸 |
14.对于反应N2+O2?2NO在密闭容器中进行,下列哪些条件能加快反应的速率( )
| A. | 缩小体积使压强增大 | B. | 体积不变充入稀有气体使压强增大 | ||
| C. | 体积不变充入He使压强增大 | D. | 压强不变充入稀有气体氖 |
12. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,用标准溶液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液由红色变为无色,且半分钟不再改变时,达到滴定终点.
(2)该小组在步骤①中的错误是锥形瓶不能用待测液润洗
由此造成的测定结果偏高(偏高、偏低或无影响)
(3)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)请根据下表数据计算待测烧碱溶液的浓度0.0800mol/L.
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,用标准溶液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液由红色变为无色,且半分钟不再改变时,达到滴定终点.
(2)该小组在步骤①中的错误是锥形瓶不能用待测液润洗
由此造成的测定结果偏高(偏高、偏低或无影响)
(3)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)请根据下表数据计算待测烧碱溶液的浓度0.0800mol/L.
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前度数(mL) | 滴定后度数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
 .
.