题目内容
16.稀氨水中存在平衡:NH3•H2O?NH4++OH_,若要使平衡逆向移动,同时使C (OH_)增大,应加入的物质或采取的措施是( )①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥MgSO4固体.
| A. | ①②③⑤ | B. | ③⑥ | C. | ③ | D. | ③⑤ |
分析 若要使平衡逆向移动,同时使c(OH-)增大,则可加入能电离出氢氧根离子的物质,结合浓度对化学平衡的影响来解答.
解答 解:①NH4Cl固体,铵根离子浓度增大,平衡逆向移动,c(OH-)减小,故错误;
②硫酸会消耗氢氧根离子,氢氧根离子浓度减小,平衡正向移动,故错误;
③NaOH固体,溶液中氢氧根离子浓度增大,电离平衡逆向移动,故正确;
④水稀释,氨水的浓度减小,平衡正向移动,氢氧根离子浓度减小,故错误;
⑤加热促进一水合氨的电离,则电离平衡正向移动,氢氧根离子浓度增大,故错误;
⑥加入少量MgSO4固体,氢氧根离子与镁离子反应生成氢氧化镁沉淀,平衡正向移动,氢氧根离子浓度减小,故错误;
故选C.
点评 本题考查电离平衡的影响因素,注意把握浓度对电离平衡的影响为解答的关键,明确逆向移动及[OH-]增大均满足即可解答,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
1. 在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
 在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )| A. | ①②③ | B. | ①③② | C. | ②①③ | D. | ②③① |
6.下列化学用语或模型表示正确的是( )
| A. | 氚原子符号:H | B. | H2O2分子结构式:H-O-O-H | ||
| C. | Mg2+结构示意图: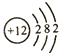 | D. | HF的形成过程 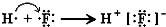 |
 .
.