题目内容
6.X、Y、Z、W为短周期元素,X2-和Y+核外电子排布相同,X、Z位于同一主族,Z、W位于同一周期,W的最外层电子数是X、Y最外层电子数之和.下列说法不正确的是( )| A. | 原子半径Y>Z>X | |
| B. | X分别与Y、Z形成的化合物均至少有两种 | |
| C. | 最高价氧化物对应水化物的酸性:W>Z | |
| D. | 氢元素在与X、Y、Z分别形成的化合物中,化合价均为+1 |
分析 X、Y、Z、W为短周期元素,X2-和Y+核外电子排布相同,则X为O,Y为Na,X、Z位于同一主族,Z为S,Z、W位于同一周期,W的最外层电子数是X、Y最外层电子数之和,则W的最外层电子数为6+1=7,W为Cl,以此来解答.
解答 解:由上述分析可知,X为O,Y为Na,Z为S,W为Cl,
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径Y>Z>X,故A正确;
B.X分别与Y、Z形成的化合物为氧化钠、过氧化钠、二氧化硫、三氧化硫,均至少有两种,故B正确;
C.非金属性W>Z,最高价氧化物对应水化物的酸性:W>Z,故C正确;
D.氢元素在与X、Y、Z分别形成的化合物中,NaH中H为-1价,水、硫化氢中H元素化合价均为+1,故D错误;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、元素的性质、原子结构来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
14.对于下列实验事实的解释,不合理的是( )
| 选项 | 实验事实 | 解释 |
| A | 加热蒸干MgSO4溶液能得到MgSO4固体;加热蒸干MgCl2溶液得不到MgCl2固体 | H2SO4不易挥发,HCl易挥发 |
| B | 电解CuCl2溶液,阴极得到Cu;电解NaCl溶液,阴极得不到Na | 得电子能力:Cu2+>Na+>H+ |
| C | 浓HNO3能氧化NO;稀HNO3不能氧化NO | HNO3浓度越大,氧化性越强 |
| D | 钠与乙醇反应平缓;钠与水反应剧烈 | 羟基中氢的活性:C2H5OH<H2O |
| A. | A | B. | B | C. | C | D. | D |
1.食盐在生活中应用广泛,下列不属于食盐用途的是( )
| A. | 着色 | B. | 防腐 | C. | 调味 | D. | 杀菌 |
11.分子式为C5H8O2,能使溴的CC14溶液褪色且分子中含有一个甲基的羧酸类物质共有(不含立体异构)( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
18.己知:图1中a和b分别为常温下盐酸和NaOH溶液互滴的pH变化曲线;图2为常温下CaSO4在水中的沉淀溶解平衡曲线.下列相关叙述正确的是( )
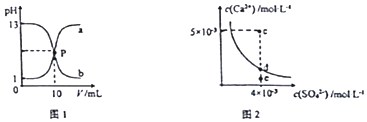

| A. | 图1中P点溶液:c(Na+ )=c(Cl-)>c(H+ )=c(OH- ) | |
| B. | 由图1可知盐酸和NaOH溶液的浓度均为1mol•L-1 | |
| C. | 图2中c点有沉淀生成,达平衡后溶液中c(SO42- )=3×10-3 mol•L-1 | |
| D. | 可通过蒸发将图 2中e点的溶液变到d点 |
15.W、X、Y、Z是短周期元素,在元素周期表中的相对位置如图所示,下列推断正确的是( )
| W | Y | |
| X | Z |
| A. | 若W的氧化物为WO2,则Z的最高价含氧酸一定为H2ZO4 | |
| B. | 若X的单质可作半导体材料,则Y的氢化物的水溶液一定显碱性 | |
| C. | 原子半径大小顺序一定为X>Z>Y>W | |
| D. | 最高正化合价大小顺序一定为Y=Z>X>W |
14.下列有关电化学的说法正确的是( )
| A. | 锌锰干电池工作一段时间后碳棒变细 | |
| B. | 在海轮外壳上镶入锌块可减缓船体的腐蚀,是采用了牺牲阳极的阴极保护法 | |
| C. | 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |