题目内容
人体健康与食品、药物等关系密切.
①合理搭配饮食是我们的健康理念.比如早餐搭配:牛奶、面包、黄油、水果等,其中含有的营养素有油脂、糖类、 、 无机盐和水.
②生活中应合理地摄取人体必需的元素,体内 元素含量过高或过低,会引起甲状腺疾病;当人体内缺钙时,可能患有的疾病是 .
a.贫血 b.骨质疏松 c.夜盲症
③氢氧化铝可以用来治疗胃酸过多,请写出该反应的离子方程式 .
④青霉素适合治疗的疾病是 .
a.感冒发烧 b.细菌感染 c.胃酸过多.
①合理搭配饮食是我们的健康理念.比如早餐搭配:牛奶、面包、黄油、水果等,其中含有的营养素有油脂、糖类、
②生活中应合理地摄取人体必需的元素,体内
a.贫血 b.骨质疏松 c.夜盲症
③氢氧化铝可以用来治疗胃酸过多,请写出该反应的离子方程式
④青霉素适合治疗的疾病是
a.感冒发烧 b.细菌感染 c.胃酸过多.
考点:常见的食品添加剂的组成、性质和作用,药物的主要成分和疗效
专题:
分析:①根据早餐食谱中的食物所含的主要营养素种类回答;
②碘元素的缺乏或含量过高,均会引起甲状腺疾病;根据钙的生理功能来判断;
③氢氧化铝是一种弱碱,可以中和胃酸;
④青霉素是一种高效、低毒、临床应用广泛的重要抗生素.它的研制成功大大增强了人类抵抗细菌性感染的能力,带动了抗生素家族的诞生.它的出现开创了用抗生素治疗疾病的新纪元.通过数十年的完善,青霉素针剂和口服青霉素已能分别治疗肺炎、肺结核、脑膜炎、心内膜炎、白喉、炭疽以及外伤感染等病.内服易被胃酸和消化酶破坏.
②碘元素的缺乏或含量过高,均会引起甲状腺疾病;根据钙的生理功能来判断;
③氢氧化铝是一种弱碱,可以中和胃酸;
④青霉素是一种高效、低毒、临床应用广泛的重要抗生素.它的研制成功大大增强了人类抵抗细菌性感染的能力,带动了抗生素家族的诞生.它的出现开创了用抗生素治疗疾病的新纪元.通过数十年的完善,青霉素针剂和口服青霉素已能分别治疗肺炎、肺结核、脑膜炎、心内膜炎、白喉、炭疽以及外伤感染等病.内服易被胃酸和消化酶破坏.
解答:
解:①根据六大营养素是指糖类、油脂、蛋白质、油脂、无机盐和水,牛奶中主要含蛋白质和水,面包中主要含糖类,还有少量的无机盐,黄油中含油脂,水果中含维生素和水,故含有的营养素除了油脂、糖类、无机盐和水,还含有蛋白质和维生素,故答案为:蛋白质,维生素;
②碘元素的含量过低或含量过高,均会引起甲状腺疾病;钙质主要存在于骨骼和牙齿中,使谷歌和牙齿具有坚硬的结构,幼儿和青少年缺钙会导致佝偻病,老年人缺钙会导致骨质疏松,故答案为:碘;b;
③氢氧化铝是一种弱碱,能中和胃酸盐酸,离子方程式为:Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3+3H+=Al3++3H2O;
④青霉素是一种高效、低毒、临床应用广泛的重要抗生素.青霉素针剂和口服青霉素已能分别治疗肺炎、肺结核、脑膜炎、心内膜炎、白喉、炭疽以及外伤感染等病.内服易被胃酸和消化酶破坏,故选b.
②碘元素的含量过低或含量过高,均会引起甲状腺疾病;钙质主要存在于骨骼和牙齿中,使谷歌和牙齿具有坚硬的结构,幼儿和青少年缺钙会导致佝偻病,老年人缺钙会导致骨质疏松,故答案为:碘;b;
③氢氧化铝是一种弱碱,能中和胃酸盐酸,离子方程式为:Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3+3H+=Al3++3H2O;
④青霉素是一种高效、低毒、临床应用广泛的重要抗生素.青霉素针剂和口服青霉素已能分别治疗肺炎、肺结核、脑膜炎、心内膜炎、白喉、炭疽以及外伤感染等病.内服易被胃酸和消化酶破坏,故选b.
点评:本题考查了六大营养元素和与生活密切相关的常识性问题,难度不大,注意知识的积累.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-.现取该溶液进行有关实验,实验结果如图所示:
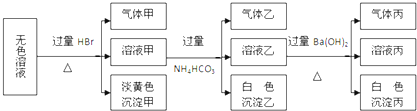
下列说法正确的是( )

下列说法正确的是( )
| A、沉淀甲可能是AgBr |
| B、沉淀丙一定是BaCO3 |
| C、气体甲的成份只有4种可能 |
| D、肯定存在的离子有AlO2-、S2-、SO32-、Na+ |
下列说法正确的是( )
A、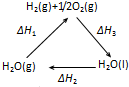 △H1=△H2+△H3 |
B、 在催化剂条件下,反应的活化能等于E1+E2 |
C、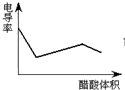 表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 |
D、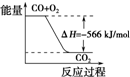 可表示由CO(g)生成CO2(g)的反应过程和能量关系 |
氢氧化钙溶解度随温度的变化如表所示,下列说法错误的是( )
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 | 150 | 200 |
| 溶解度(g/100gH2O) | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.11 | 0.092 | 0.074 | 0.034 | 0.012 |
| A、氢氧化钙的溶解是放热过程 |
| B、100℃时氢氧化钙的Kxp约等于4×10-6 |
| C、温度升高时氢氧化钙溶解速率加快 |
| D、100℃时pH=12的溶液中c(Ca2+)≤0.04mol?L-1 |
 是一种新型可生物降解的高分子材料,主要用于制造可降解纤维,可降解塑料和医用材料.它以淀粉为原料,先水解为葡萄糖,再在乳酸菌的作用下降葡萄糖转变为乳酸
是一种新型可生物降解的高分子材料,主要用于制造可降解纤维,可降解塑料和医用材料.它以淀粉为原料,先水解为葡萄糖,再在乳酸菌的作用下降葡萄糖转变为乳酸 ,乳酸在催化剂的催化下聚合成聚乳酸.聚乳酸材料废弃后,先水解成乳酸,乳酸在微生物的作用下分解为CO2和H2O.请用化学方程式表示上述聚合与降解的过程.
,乳酸在催化剂的催化下聚合成聚乳酸.聚乳酸材料废弃后,先水解成乳酸,乳酸在微生物的作用下分解为CO2和H2O.请用化学方程式表示上述聚合与降解的过程.
 某溶液中可能含有的离子如下表:
某溶液中可能含有的离子如下表: