题目内容
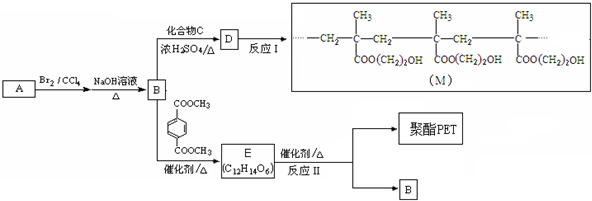
化合物X是一种环境激素,存在如下转化关系:

化合物A能与FeCl3溶液发生显色反应,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取代物只有两种.B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应.F( DMAEMA)在日化行业中常用于制备润湿剂、分散剂、树脂添加剂等.
已知:RCOOR'+R”18OH
RCO18OR+R'OH( R、R′、R″代表烃基)根据以上信息回答:
(1)B的官能团名称是 ,A→C的反应类型是 .
(2)写出B在一定条件发生缩聚反应的方程式 .
(3)写出B→G反应的化学方程式 .
(4)同时满足下列条件的D的同分异构体有 种(包括顺反异构),写出其中一种的结构简式 .
a.属于酯类 b.能发生银镜反应 c.不含环状结构
(5),写出E→F反应的化学方程式 .
(6)下列叙述正确的是 (填字母).
a.化合物E不能与Br2发生加成反应
b.化合物A可以和NaHCO3溶液反应
c.X与NaOH溶液反应,理论上1mol X最多消耗6mol NaOH
(7)X的结构简式为 .

化合物A能与FeCl3溶液发生显色反应,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取代物只有两种.B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应.F( DMAEMA)在日化行业中常用于制备润湿剂、分散剂、树脂添加剂等.
已知:RCOOR'+R”18OH
| 催化剂 |
| △ |
(1)B的官能团名称是
(2)写出B在一定条件发生缩聚反应的方程式
(3)写出B→G反应的化学方程式
(4)同时满足下列条件的D的同分异构体有
a.属于酯类 b.能发生银镜反应 c.不含环状结构
(5),写出E→F反应的化学方程式
(6)下列叙述正确的是
a.化合物E不能与Br2发生加成反应
b.化合物A可以和NaHCO3溶液反应
c.X与NaOH溶液反应,理论上1mol X最多消耗6mol NaOH
(7)X的结构简式为
考点:有机物的推断
专题:有机物的化学性质及推断
分析:根据A能与FeCl3溶液发生显色反应可知A中含有酚羟基,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取代物只有两种,再结合A→C转化条件和A、C分子式可知A中含有两个苯环,故A结构简式为: ,A发生取代反应生成C为
,A发生取代反应生成C为 ;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为:
;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为: ,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为
,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为 ,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为
,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为 ,G为
,G为 ,据此答题.
,据此答题.
 ,A发生取代反应生成C为
,A发生取代反应生成C为 ;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为:
;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为: ,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为
,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为 ,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为
,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为 ,G为
,G为 ,据此答题.
,据此答题.解答:
解:根据A能与FeCl3溶液发生显色反应可知A中含有酚羟基,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取代物只有两种,再结合A→C转化条件和A、C分子式可知A中含有两个苯环,故A结构简式为: ,A发生取代反应生成C为
,A发生取代反应生成C为 ;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为:
;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为: ,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为
,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为 ,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为
,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为 ,G为
,G为 ,
,
(1)B的结构简式为 ,所以B的官能团名称是羟基和羧基,A→C的反应类型是取代反应,
,所以B的官能团名称是羟基和羧基,A→C的反应类型是取代反应,
故答案为: ;取代反应;
;取代反应;
(2)B在一定条件发生缩聚反应的方程式为 ,
,
故答案为: ;
;
(3)B→G反应的化学方程式为 ,
,
故答案为: ;
;
(4)同时满足下列条件a.属于酯类,b.能发生银镜反应,即有醛基,c.不含环状结构,符合这些条件的D的同分异构体有 ,共4种(包括顺反异构),其中一种的结构简式为
,共4种(包括顺反异构),其中一种的结构简式为 ,
,
故答案为:4; ;
;
(5)E→F反应的化学方程式为 ,
,
故答案为: ;
;
(6)下列叙述中,
a.E为CH2=C(CH3)COOCH2CH2OH,能与Br2发生加成反应,故a错误;
b.化合物A中没有羧基,不能和NaHCO3溶液反应,故b错误;
c.X中有两个酚酯和两个溴原子,与NaOH溶液发生水解反应,理论上1mol X最多消耗6mol NaOH,故c正确;
故答案为:c;
(7)根据上面的分析可知,X的结构简式为 ,
,
故答案为: .
.
 ,A发生取代反应生成C为
,A发生取代反应生成C为 ;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为:
;由此推出B中必含羧基,X为酚酯.再利用B→D与B→G反应可知B中还含有羟基,其中B→D发生的是消去反应、B→G发生的是酯化反应(生成环酯),B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应,说明B中有羧基,可知B的结构简式为: ,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为
,再利用反应①(酯的水解反应)和X的分子式,可推出X的结构简式为 ,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为
,进而可利用框图转化,结合有机物的性质由B可推知D为CH2=C(CH3)COOH,E为CH2=C(CH3)COOCH2CH2OH,F为 ,G为
,G为 ,
,(1)B的结构简式为
 ,所以B的官能团名称是羟基和羧基,A→C的反应类型是取代反应,
,所以B的官能团名称是羟基和羧基,A→C的反应类型是取代反应,故答案为:
 ;取代反应;
;取代反应;(2)B在一定条件发生缩聚反应的方程式为
 ,
,故答案为:
 ;
; (3)B→G反应的化学方程式为
 ,
,故答案为:
 ;
;(4)同时满足下列条件a.属于酯类,b.能发生银镜反应,即有醛基,c.不含环状结构,符合这些条件的D的同分异构体有
 ,共4种(包括顺反异构),其中一种的结构简式为
,共4种(包括顺反异构),其中一种的结构简式为 ,
,故答案为:4;
 ;
;(5)E→F反应的化学方程式为
 ,
,故答案为:
 ;
;(6)下列叙述中,
a.E为CH2=C(CH3)COOCH2CH2OH,能与Br2发生加成反应,故a错误;
b.化合物A中没有羧基,不能和NaHCO3溶液反应,故b错误;
c.X中有两个酚酯和两个溴原子,与NaOH溶液发生水解反应,理论上1mol X最多消耗6mol NaOH,故c正确;
故答案为:c;
(7)根据上面的分析可知,X的结构简式为
 ,
,故答案为:
 .
.
点评:本题通过有机框图转化考查有机化学知识,意在考查考生对知识的应用和综合思维能力,题目难度中等,解答本题的关键是利用题中信息和有机物间转化关系图确定出各物质的结构简式,然后再回答有关问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一定条件下水分解生成氢气和氧气,有关物质和能量的转化关系如图所示,下列判断正确的是( )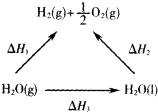

| A、△H1>△H2 |
| B、△H2<△H3 |
| C、△H1=△H2+△H3 |
| D、△H1+△H3>△H2 |
下列有机物用于合成聚乙烯塑料,是聚乙烯的单体的是( )
| A、CH4 |
| B、CH2=CH2 |
| C、CH3CH2OH |
| D、CH2=CHCH3 |
短周期元素X、Y、Z在元素周期表中的相对位置所示,其中X原子最外层电子数是次外层电子数的3倍.下列说法错误的是( )
| X | |
| Y | Z |
| A、元素X和元素Y的最高正化合价相同 |
| B、气态氢化物的热稳定性:H2Y<H2X |
| C、Y2Z2是共价化合物 |
| D、酸性:HZO4>H2YO4 |
 次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,具有较强还原性.
次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,具有较强还原性.

