题目内容
单质A、B、C在一定条件下,可以按下面的流程进行反应.已知单质A、B常温下分别为无色气体和黄绿色气体,单质C是常见的金属,D的水溶液常温下能与单质C反应生成F和单质A.
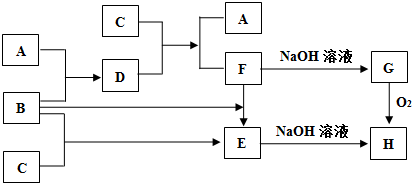
请完成下列填空:
(1)写出单质B的化学式 ,D物质的电子式 .
(2)写出E→H的化学方程式 .
(3)写出D+C→F+A的离子方程式 .

请完成下列填空:
(1)写出单质B的化学式
(2)写出E→H的化学方程式
(3)写出D+C→F+A的离子方程式
考点:无机物的推断
专题:推断题
分析:B为黄绿色气体单质,所以B为氯气,A为无色气体,A与氯气反应生成D,D与金属C反应又得A,所以A为氢气,D为氯化氢,F为含C金属元素的盐,G为C金属元素的碱,B、C反应生成E,E与碱反应生成H,G氧化得H,说明C中含有的金属元素为可变价元素,C是常见的金属,据此可推知C为铁,F为氯化亚铁,G为氢氧化亚铁,E为氯化铁,H为氢氧化铁,据此答题.
解答:
解:B为黄绿色气体单质,所以B为氯气,A为无色气体,A与氯气反应生成D,D与金属C反应又得A,所以A为氢气,D为氯化氢,F为含C金属元素的盐,G为C金属元素的碱,B、C反应生成E,E与碱反应生成H,G氧化得H,说明C中含有的金属元素为可变价元素,C是常见的金属,据此可推知C为铁,F为氯化亚铁,G为氢氧化亚铁,E为氯化铁,H为氢氧化铁,
(1)根据上面的分析可知,单质B的化学式为Cl2,D为氯化氢,D物质的电子式 ,故答案为:Cl2;
,故答案为:Cl2; ;
;
(2)E→H的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl,故答案为:FeCl3+3NaOH═Fe(OH)3↓+3NaCl;
(3)D+C→F+A的离子方程式为Fe+2H+=2Fe2++H2↑,故答案为:Fe+2H+=2Fe2++H2↑.
(1)根据上面的分析可知,单质B的化学式为Cl2,D为氯化氢,D物质的电子式
 ,故答案为:Cl2;
,故答案为:Cl2; ;
;(2)E→H的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl,故答案为:FeCl3+3NaOH═Fe(OH)3↓+3NaCl;
(3)D+C→F+A的离子方程式为Fe+2H+=2Fe2++H2↑,故答案为:Fe+2H+=2Fe2++H2↑.
点评:本题考查无机物的推断,主要考查了铁及其化合物性质的应用,题目难度中等,本题注意推断Fe为解答该题的关键,“黄绿色气体”为突破口.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
某有机物的分子式为C8H8O2,含有苯环和-COOH的同分异构体有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
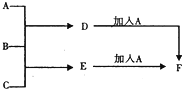 A、B、C为3种单质(其中A为固体,B、C为气体),将D的饱和溶液滴人沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E.它们之间的转化关系如图,下列推断正确的是( )
A、B、C为3种单质(其中A为固体,B、C为气体),将D的饱和溶液滴人沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E.它们之间的转化关系如图,下列推断正确的是( )| A、物质B是H2 |
| B、物质C是Cl2 |
| C、物质D是FeCl2 |
| D、物质F是FeCl2 |
设NA是阿伏伽德罗常数的数值,下列说法正确的是( )
| A、1L 1mol?L-1的Na2CO3 溶液中含有CO32-的数目为NA |
| B、常温常压下,22.4 L CH4中含有4 NA 个C-H键 |
| C、常温常压下,1.7gH2O2中含有的电子数为0.5 NA |
| D、1 mol Zn与足量稀HNO3反应,转移2NA个电子 |



