题目内容
5.X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素,其中只有Z是金属元素,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示.下列说法中正确的是( )| X | Y | |||
| W |
| A. | 五种元素中,原子半径最大的是W | |
| B. | Y 的氧化性比W的氧化性强 | |
| C. | Y与Z形成的化合物都可以和水反应 | |
| D. | Z与Q形成的化合物一定是离子化合物 |
分析 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.W的单质是黄色固体,则W为S,可推知Q为Cl,由X、Y、W在周期表中的相对位置,可知X为C、Y为O,其中只有Z是金属,则Z可能为Na或Mg或Al,以此来解答.
解答 解:X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.W的单质是黄色固体,则W为S,可推知Q为Cl,由X、Y、W在周期表中的相对位置,可知X为C、Y为O,其中只有Z是金属,则Z可能为Na或Mg或Al,
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径:Z>W>Q>X>Y,故A错误;
B.非金属性Y大于W,故Y 的氧化性比W的氧化性强,故B正确;
C.氧化镁、氧化铝都不能与水反应,故C错误;
D.A为Al时,与Q形成的化合物为AlCl3,属于共价化合物,故D错误;
故选B.
点评 本题考查位置、结构与性质的综合应用,为高频考点,把握W单质的颜色推断各元素为解答的关键,侧重分析与应用能力的考查,注意Z不确定,题目难度不大.

练习册系列答案
相关题目
15.近年来,科学家研制出一种新型的乙醇电池,它用酸性电解质(H+)作溶剂.电池总反应为 C2H5OH+3O2═2CO2+3H2O,下列说法不正确的是( )
| A. | 乙醇在电池的负极上参加反应 | |
| B. | 1 mol C2H5OH被氧化时,有6 mol电子转移 | |
| C. | 随着反应的进行,正极附近溶液的酸性减弱 | |
| D. | 电池的正极反应为2H2O+O2+4e- 4OH- |
16.在下列化学反应中,既有离子键、共价键断裂,又有离子键、共价键形成的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | SO2+2H2S═3S↓+2H2O | ||
| C. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
13.分子式为CnH2n+1X(n≠1)的卤代烃不能发生消去反应,n的最小值是( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
20.下列反应既属于氧化还原反应,又是吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 水分解生成氢气和氧气 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
10.下列说法正确的是( )
| A. | 0.1mol•L-1的醋酸加水稀释,$\frac{c({H}^{+})}{c(O{H}^{-})}$减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 | |
| C. | 体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 | |
| D. | 常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性 |
17.化学科学需要借助化学专用语言来描述,下列有关化学用语不正确的是( )
| A. | 甲烷分子的球棍模型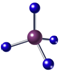 | |
| B. | Cl-的结构示意图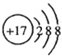 | |
| C. | 中子数为8的碳原子的核素符号为12C | |
| D. | 中子数为1的氢原子的核素符号为21H |
 .
.