题目内容
17.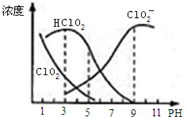 亚氯酸钠是一种高效氧化剂漂白剂,主要用于 棉纺、亚麻、纸浆等漂白亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )
亚氯酸钠是一种高效氧化剂漂白剂,主要用于 棉纺、亚麻、纸浆等漂白亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )| A. | 亚氯酸钠在碱性条件下较稳定 | |
| B. | 25℃时,HClO2的电离平衡常数的数值Ka=10-6 | |
| C. | 使用该漂白剂的最佳pH为3 | |
| D. | 25℃时,同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) |
分析 A、由图可以得出:碱性条件下ClO2-浓度高;
B、HClO2的电离平衡常数K=$\frac{c({H}^{+})c(ClO{{\;}_{2}}^{-})}{c(HClO2)}$结合图示数据来计算;
C、根据题意:HClO2和ClO2都具有漂白作用,结合图中HClO2和ClO2的浓度大小来确定使用该漂白剂的最佳pH;
D、依据电中性原则得出:c(H+)+c(Na+)=c(ClO2-)+c(OH-),依据物料守恒得出:2c(Na+)=c(ClO2-)+c(HClO2),据此解答即可.
解答 解:A、由图可以得出:碱性条件下ClO2-浓度高,即在碱性条件下亚氯酸钠较稳定,故A正确;
B、HClO2的电离平衡常数K=$\frac{c({H}^{+})c(ClO{{\;}_{2}}^{-})}{c(HClO2)}$=10-3×10-3=10-6,故B正确;
C、考虑二氧化氯是有毒气体,浓度高时不宜使用,故pH应该为4-5,此时,二氧化氯浓度较低,且亚氯酸浓度不是很低,使用最佳,故C错误;
D、依据电中性原则得出:c(H+)+c(Na+)=c(ClO2-)+c(OH-) ①,依据物料守恒得出:2c(Na+)=c(ClO2-)+c(HClO2) ②,联立①②消去钠离子:c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-),故D正确,
故选C.
点评 本题考查了酸碱混合的定性判断,题目难度稍大,正确分析、理解题中信息及图象数据是解答本题关键,注意明确溶液酸碱性与溶液pH的关系.

练习册系列答案
相关题目
8.几种短周期元素的原子半径及某些化合价见下表.分析判断下列说法正确的是( )
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | I在DB2中燃烧生成两种化合物 | |
| B. | B、E、J的离子半径由大到小顺序是E>J>B | |
| C. | G元素的单质不存在同素异形体 | |
| D. | B和J能形成既含离子键又含共价键的化合物 |
5.五倍子是一种常见的中草药,其有效成分为X.在一定条件下X可分别转化为Y、Z.下列说法错误的是( )
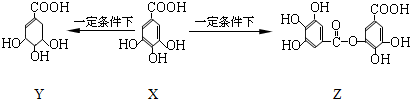

| A. | 1 mol X最多能与2 mol Br2发生取代反应 | |
| B. | Y分子结构中有3个手性碳原子 | |
| C. | Y能发生加成、取代、消去、氧化 | |
| D. | 1 mol Z最多能与7 mol NaOH发生反应 |
12.可以把5种无色溶液:乙醇、苯酚、AgNO3溶液、KOH溶液区分的试剂是( )
| A. | 新制碱性Cu(OH)2悬浊液 | B. | FeCl3溶液 | ||
| C. | BaCl2溶液 | D. | 酸性KMnO4溶液 |
2.下列物质的化学式能表示分子式的是( )
| A. | NaCl | B. | SiO2 | C. | Ar | D. | Na |
9.下列叙述正确的是( )
| A. | 分子晶体中的每个分子内一定含有共价键 | |
| B. | 金属晶体的熔点和沸点都很高 | |
| C. | 离子晶体中可能含有共价键 | |
| D. | 原子晶体中的相邻原子间只存在非极性共价键 |
6.酒后驾车是引发交通事故的重要原因.交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+.下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物.
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物.
| A. | ②④ | B. | ②③ | C. | ①③ | D. | ①④ |
7.下列措施肯定能使化学反应速率增大的是( )
①增大反应物的量 ②减小压强 ③升高温度 ④使用正催化剂.
①增大反应物的量 ②减小压强 ③升高温度 ④使用正催化剂.
| A. | ①②③ | B. | ③④ | C. | ②③④ | D. | ①②③④ |