题目内容
4.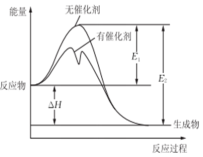 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )| A. | 该反应为吸热反应 | |
| B. | E1-E2=△H | |
| C. | 升高温度,不会提高活化分子的百分数 | |
| D. | 使用催化剂使该反应的化学平衡常数发生改变 |
分析 A.由图可知,反应物总能量大于生成物总能量;
B.焓变等于正逆反应活化能之差;
C.升高温度,提供能量,增大活化分子百分数;
D.K与温度有关.
解答 解:A.由图可知,反应物总能量大于生成物总能量,则正反应为放热反应,故A错误;
B.焓变等于正逆反应活化能之差,则E1-E2=△H,故B正确;
C.升高温度,提供能量,增大活化分子百分数,反应速率加快,故C错误;
D.K与温度有关,则使用催化剂使该反应的化学平衡常数不变,故D错误;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握图中能量变化、温度和催化剂对反应的影响为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列图示的实验操作,能实现相应实验目的是( )
| A. |  蒸干CuCl2饱和溶液制备无水CuCl2 | |
| B. | 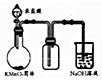 实验室制取并收集少量纯净氯气 | |
| C. | 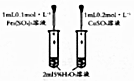 研究催化剂对H2O2分解速率的影响 | |
| D. | 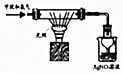 验证甲烷和氧气光照条件下发生取代反应 |
15.短周期主族元素X、Y、Z、U、W原子序数依次增大,X位于 IA族,Y原子最外层电子数是其内层电子数的2倍,Z的简单气态氢化物的稳定性最强,U是地壳中含量最多的金属元素,W与Z属于同一主族,下列叙述正确的是( )
| A. | 由X与W形成的化合物是离子化合物 | |
| B. | Z元素的最低化合价为-1,最高化合价为+7 | |
| C. | Y的最高价氧化物对应水化物的酸性比U的强 | |
| D. | Z的简单离子半径小于U的简单阳离子半径 |
12.化学与生产、生活密切相关,下列有关说法正确的是( )
| A. | 沼气是可再生资源,电能是二次能源 | |
| B. | 对“地沟油”进行蒸馏即可得到汽油 | |
| C. | 用焦炭还原铝土矿即可获得金属铝 | |
| D. | 从海水提取物质都必须通过化学反应方可实现 |
19.下列有关物质的性质与用途具有对应关系的是( )
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | 碳酸氢钠能与碱反应,可用作食品的膨松剂 | |
| C. | 四氯化碳密度比水大,可用于萃取溴水中的Br2 | |
| D. | MgO、Al2O3的熔点都很高,都可用作耐火材料 |
9.根据下列实验操作与现象所得到的结论正确的是( )
| 选项 | 实验操作与现象 | 结论 |
| A | 向蛋白质溶液中滴加Pb(NO3)2溶液,产生白色沉淀,加水沉淀不消失 | 蛋白质发生了变性 |
| B | 测定浓度为 0.1mol•L-1CH3COONa与HCOONa 溶液的pH,CH3COONa溶液的pH较大 | 酸性:CH3COOH>HCOOH |
| C | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀 | 溶液X中一定含有SO42- |
| D | 向浓度均为0.1mol•L-1NaCl和NaI混合溶液中滴加少量0.l mol•L-1AgNO3溶液,出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| A. | A | B. | B | C. | C | D. | D |
7.科技工作者制造出厚度只有l微米的超薄太阳能电池.硅太阳能电池工作原理如图所示:

下列有关判断错误的是( )

下列有关判断错误的是( )
| A. | 硅原子最外层有4个电子 | |
| B. | 太阳能电池是一种化学电源 | |
| C. | 太阳能电池实现了光能向电能的转化 | |
| D. | B电极为电源正极 |
4.下列表示正确的是( )
| A. | -CH3(甲基)的电子式为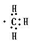 | B. | 乙烯分子的结构简式:CH2CH2 | ||
| C. | H2O分子的球棍模型: | D. | 氟的原子结构示意图: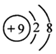 |
5.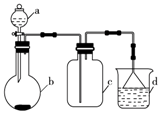 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 浓硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |