题目内容
5.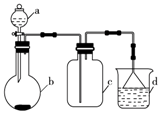 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 浓硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 题给装置在常温下反应生成气体,且用向上排空气法收集,说明气体密度比空气大,最后为防倒吸装置,以此解答该题.
解答 解:A.浓氨水与氧化钙混合生成氨气,氨气的密度比空气小,不能使用向上排空气法,故A错误;
B.浓硫酸与亚硫酸钠反应生成二氧化硫,二氧化硫密度大于空气,浓硫酸能够干燥二氧化硫气体,故B正确;
C.二氧化氮和水反应生成NO,不能用水吸收尾气,故C错误;
D.常温下浓盐酸和二氧化锰不反应,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及常见气体的制备原理、收集及尾气处理等,把握实验原理及实验技能为解答的关键,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
4.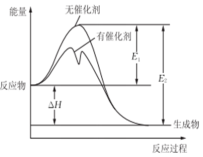 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )
 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )| A. | 该反应为吸热反应 | |
| B. | E1-E2=△H | |
| C. | 升高温度,不会提高活化分子的百分数 | |
| D. | 使用催化剂使该反应的化学平衡常数发生改变 |
16.已知2L 0.5mol/L H2SO4溶液与足量稀NaOH溶液反应,放出114.6kJ的热量,表示该反应中和热的热化学方程式正确的是( )
| A. | H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l)△H=-114.6 kJ•mol-1 | |
| B. | H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l)△H=+114.6 kJ•mol-1 | |
| C. | $\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=+57.3 kJ•mol-1 | |
| D. | $\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ•mol-1 |
13.下列实验现象描述或观点正确的是( )
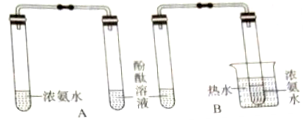

| A. | 将品红溶液滴入饱和亚硫酸溶液后,溶液红色褪去 | |
| B. | 向饱和FeCl3溶液加入适量的浓氨水,所得红褐色物质就是胶体 | |
| C. | A酚酞溶液变红,B装置中酚酞溶液不变色 | |
| D. | 金属钠、溴水和紫色石蕊溶液均可用来鉴别苯、乙醇、乙酸 |
20.某研究性学习小组为测定花溪河水中 Ca2+的含量,取样 100mL,经测定其中含 Ca2+的质量为 4mg,则该河水中 Ca的物质的量浓度为( )
| A. | 1×10-4mol/L | B. | 1×10-3mol/L | C. | 4×10-4mol/L | D. | 4×10-3mol/L |
10.X、Y、Z、W、R是原了序数依次递增的短周期元素.X原子最外层电子数是其内层电子数的2倍,Y、R同主族,且两者核外电子数之和是X核外电子数的4倍,Z为短周期中金属性最强的元素,W是地売中含量最高的金属元素.下列叙述正确的是( )
| A. | Y、Z、W原子半径依次增大 | |
| B. | X的最高价氧化物对应水化物的酸性比R的强 | |
| C. | X、R分别与Y形成的常见化合物中化学键类型相同 | |
| D. | 元素W、R的简单离子具有相同的电子层结构 |
17.柠檬烯是一种食用香料,其结构简式为: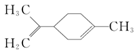 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )
 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )| A. | 它在核磁共振氢谱中有6个峰 | B. | 它能发生取代、加成和氧化反应 | ||
| C. | 它与丁基苯互为同分异构体 | D. | 它属于芳香族化合物 |
1.一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
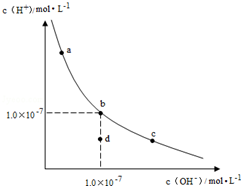

| A. | 升高温度,可能引起由c向b的变化 | |
| B. | 该温度下,水的离子积常数为1.0×10-13 | |
| C. | 该温度下,加入HCl溶液可能引起由b向a的变化 | |
| D. | 该温度下,稀释溶液可能引起由c向d的变化 |
2.下列实验操作或说法正确的是( )
| A. | 取4g NaOH加入100mL水中配制浓度为1.0mol/L的NaOH溶液 | |
| B. | 配制一定浓度的溶液时,用蒸馏水润洗容量瓶会使所配制出的溶液浓度偏低 | |
| C. | 除去Fe(OH)3胶体中混有的Cl-离子,可用过滤的方法 | |
| D. | 向盛有铜片的试管中加入浓硫酸,加热证明浓硫酸具有强氧化性 |