题目内容
14.下列图示的实验操作,能实现相应实验目的是( )| A. |  蒸干CuCl2饱和溶液制备无水CuCl2 | |
| B. | 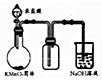 实验室制取并收集少量纯净氯气 | |
| C. | 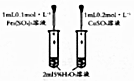 研究催化剂对H2O2分解速率的影响 | |
| D. | 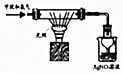 验证甲烷和氧气光照条件下发生取代反应 |
分析 A.CuCl2饱和溶液在加热时易水解;
B.盐酸易挥发;
C.研究催化剂对反应的速率的影响,过氧化氢的浓度应相同;
D.氯气与硝酸银溶液也反应.
解答 解:A.CuCl2为强酸弱碱盐,易水解生成氯化氢,氯化氢挥发,得到氢氧化铜,应在氯化氢的氛围中蒸发,故A错误;
B.因盐酸易挥发,收集到的氯气中混有氯化氢,故B错误;
C.研究催化剂对反应的速率的影响,过氧化氢的浓度应相同,可达到实验目的,故C正确;
D.氯气与硝酸银溶液也反应,不能证明发生取代反应,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及盐类的水解、气体的制备以及反应速率的影响因素等,把握实验原理及实验装置图的作用为解答的关键,注意方案的合理性、操作性分析,题目难度不大.

练习册系列答案
相关题目
2.随着人们对物质组成和性质研究的深入,物质的分类也更加多样化.下列有关说法正确的是( )
| A. | H2SO4、NaOH、NaNO3都是强电解质 | B. | Na2O、Al2O3、Fe2O3都是碱性氧化物 | ||
| C. | 铝土矿、小苏打都是混合物 | D. | 烧碱、纯碱、熟石灰都是碱 |
5.下列有关说法正确的是( )
| A. | 室温时,0.1 mol•L-1某一元酸在水中有0.1%电离,此酸的电离平衡常数约为1×10-7 | |
| B. | 反应CO(g)+3H2(g)=CH4(g)+H2O(g)一定条件下可自发进行,则该反应的△H>0 | |
| C. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 | |
| D. | 为减小中和滴定误差,锥形瓶和滴定管必须洗净并润洗后才能使用 |
9.设NA为阿伏伽德罗常数值.下列有关叙述不正确的是( )
| A. | 5.8g熟石膏(2CaSO4•H2O)含有的结晶水分子数为0.02NA | |
| B. | 1mol CnH2n-2(n≥2)中所含的共用电子对数为(3n+1)NA | |
| C. | 60克的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2 | |
| D. | 在K37ClO3+6H35Cl(浓)═KCl+3Cl2↑+3H2O反应中,若有212克氯气生成,则反应中电子转移的数目为5NA |
19.下列关于有机物X(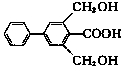 )的说法正确的是.
)的说法正确的是.
 )的说法正确的是.
)的说法正确的是.| A. | 分子式为C15H19O4 | |
| B. | 苯环上的一氯代物有7种 | |
| C. | 能发生氧化反应和取代反应 | |
| D. | 1molX与足量的NaOH溶液反应,最多消耗3molNaOH |
6.下列指定反应的离子方程式正确的是( )
| A. | 向MgCl2溶液中滴加过量氨水:Mg2++2OH-═Mg(OH)2↓ | |
| B. | 用稀硝酸洗涤试管内壁的银镜:Ag+4H++NO3-═Ag++NO↑+2H2O | |
| C. | 将Cu粉加入到Fe2(SO4)3溶液中:2Fe3++3Cu═2Fe+3Cu2+ | |
| D. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
3.下列有关物质的性质与用途具有对应关系的是( )
| A. | 石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 | |
| B. | Al具有良好的延展性和抗腐蚀性,常用铝箔包装物品 | |
| C. | 浓H2SO4溶液能使蛋白质发生盐析,可用于杀菌消毒 | |
| D. | 铜的金属活动性比铁的弱,可在海外轮外壳上装若干铜块以减缓其腐蚀 |
4.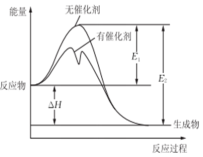 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )
 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能.下列有关叙述正确的是( )| A. | 该反应为吸热反应 | |
| B. | E1-E2=△H | |
| C. | 升高温度,不会提高活化分子的百分数 | |
| D. | 使用催化剂使该反应的化学平衡常数发生改变 |