题目内容
17.硫酸锌被广泛应用于医药领域和工农业生产.工业上由氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)生产ZnSO4•7H2O的一种流程如图: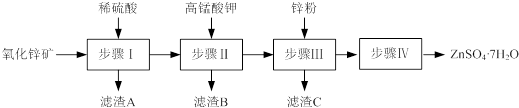
(1)步骤Ⅰ的操作是过滤,滤渣A的主要成分是H2SiO3.
(2)步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是H2SiO3+2NaOH=Na2SiO3+2H2O.
(3)步骤Ⅱ中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO(OH)2两种沉淀,该反应的离子方程式为3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+.
(4)步骤Ⅲ中,加入锌粉的作用是换出Cu,除去Cu2+.所得的滤液中含有的金属阳离子有Zn2+、K+.
(5)已知硫酸锌的溶解度与温度之间的关系如下表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
烘干操作需在减压低温条件下进行,原因是降低烘干的温度,防止ZnSO4•7H2O分解.
(6)取28.70g ZnSO4•7H2O加热至不同温度,剩余固体的质量变化如图所示.
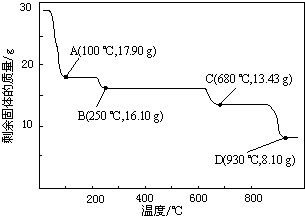
分析数据,680℃时所得固体的化学式为b.
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O.
分析 氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)加稀硫酸溶解,过滤,滤液中含有硫酸锌、硫酸铜、硫酸亚铁,再加高锰酸钾溶液与亚铁离子反应生成MnO(OH)2和氢氧化铁沉淀,过滤,滤液中含有硫酸铜和硫酸锌,加锌粉置换铜离子,过滤,滤渣为Cu可能含有Zn,滤液为硫酸锌和硫酸钾,蒸发浓缩、冷却结晶、过滤得到ZnSO4•7H2O晶体;
(1)分离固体和液体通常用过滤的方法,ZnSiO3、与稀硫酸反应生成硅酸不溶于水;
(2)用氢氧化钠溶液清洗过滤装置,目的是使反应生成的H2SiO3滤渣反应生成Na2SiO3溶解除去;
(3)高锰酸钾与Fe2+反应生成Fe(OH)3和MnO(OH)2;
(4)步骤Ⅲ:向滤液中加入锌粉,置换出铜,滤液为硫酸锌和硫酸钾;
(5)从溶液中获得晶体通常用蒸发浓缩、过滤结晶、过滤、洗涤、烘干等操作,由于ZnSO4•7H2O易分解,所以烘干操作需在减压低温条件下进行;
(6)28.70 g ZnSO4•7H2O的物质的量为0.1mol,由Zn元素守恒可知,生成ZnSO4•H2O或ZnSO4或ZnO或Zn3O(SO4)2时,物质的量均为0.1mol,根据它们的质量通过排除法确定.
解答 解:氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)加稀硫酸溶解,过滤,滤液中含有硫酸锌、硫酸铜、硫酸亚铁,再加高锰酸钾溶液与亚铁离子反应生成MnO(OH)2和氢氧化铁沉淀,过滤,滤液中含有硫酸铜和硫酸锌,加锌粉置换铜离子,过滤,滤渣为Cu可能含有Zn,滤液为硫酸锌和硫酸钾,蒸发浓缩、冷却结晶、过滤得到ZnSO4•7H2O晶体;
(1)分离固体和液体通常用过滤的方法,ZnSiO3、与稀硫酸反应生成硅酸不溶于水,
故答案为:过滤;H2SiO3;
(2)滤渣A为硅酸沉淀,用氢氧化钠溶液清洗过滤装置,目的是使反应生成的H2SiO3滤渣与氢氧化钠反应生成Na2SiO3溶解除去,其发生的反应为:H2SiO3+2NaOH=Na2SiO3+2H2O,故答案为:H2SiO3+2NaOH=Na2SiO3+2H2O;
(3)在pH约为5.1的滤液中加入高锰酸钾,高锰酸钾与Fe2+发生氧化还原反应,生成Fe(OH)3和MnO(OH)2两种沉淀,则反应的离子方程式为:3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+,
故答案为:3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+;
(4)步骤Ⅲ:向滤液中加入锌粉,置换出铜,滤液为硫酸锌和硫酸钾,所以滤液中含有的金属阳离子有Zn2+、K+,
故答案为:置换出Cu,除去Cu2+;Zn2+、K+;
(5)从溶液中获得晶体通常用蒸发浓缩、过滤结晶、过滤、洗涤、烘干等操作,由于ZnSO4•7H2O易分解,所以烘干操作需在减压低温条件下进行,
故答案为:60℃条件下蒸发浓缩、降温结晶;降低烘干的温度,防止ZnSO4•7H2O分解;
(6)28.70 g ZnSO4•7H2O的物质的量为0.1mol,由Zn元素守恒可知,生成ZnSO4•H2O或ZnSO4或ZnO或Zn3O(SO4)2时,物质的量均为0.1mol,
若得ZnSO4•H2O的质量为17.90g(100℃);
若得ZnSO4的质量为16.10g(250℃);
若得ZnO的质量为8.10g(930℃);
据此通过排除法确定680℃时所得固体的化学式为Zn3O(SO4)2;
故答案为:b.
点评 本题以ZnSO4•7H2O的制备为知识背景,考查了基本实验操作、氧化还原反应、化学反应速率的影响因素、化学方程式的书写、计算等知识,题目难度中等,侧重于考查学生的分析能力和实验能力.

| A. | NH4H是离子化合物,含有离子键和共价键 | |
| B. | NH4H与水反应时,NH4H是还原剂 | |
| C. | NH4H投入少量的水中,有两种气体产生 | |
| D. | NH4H溶于水,所形成的溶液成酸性 |
| A. | 冰雪融化 | B. | 纸张燃烧 | C. | 水分蒸发 | D. | 矿石粉碎 |
| A. | 1:1:1 | B. | 3:2:3 | C. | 1:4:1 | D. | 3:2:1 |
| A. | NH3易液化,液氨常作制冷剂 | |
| B. | NO、NO2都是有毒气体 | |
| C. | 铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 稀HNO3和活泼金属反应时主要得到氢气 |
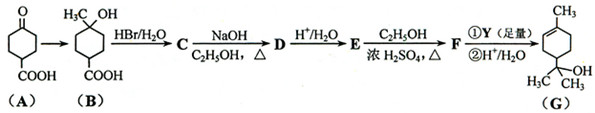
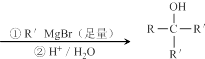
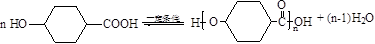 .
.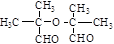 .
.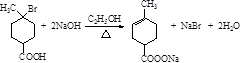 .
.
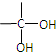 $\stackrel{自动脱水}{→}$
$\stackrel{自动脱水}{→}$
 .
. .
.