题目内容
2.x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下V L的x、y、z的混合气体可与V L的H2发生加成反应,则混合气体中x、y、z的体积比不可能是( )| A. | 1:1:1 | B. | 3:2:3 | C. | 1:4:1 | D. | 3:2:1 |
分析 烷烃不与H2反应,1 mol烯烃可与1 molH2加成,而1mol炔烃可与2 molH2加成,由于VL混合气体与VL氢气发生加成反应,因此,只要烷烃与炔烃的体积比为1:1,即符合题意,据此进行解答.
解答 解:烷烃不与H2反应,1 mol烯烃可与1 molH2加成,而1mol炔烃可与2 molH2加成,由于VL混合气体与VL氢气发生加成反应,因此,只要烷烃与炔烃的体积比为1:1,即符合题意,与烯烃的体积无关,选项中A、C、B符合,D不符合,
故选D.
点评 本题考查混合物反应的计算、化学方程式的计算,题目难度中等,根据加成反应确定烷烃与炔烃的体积比为1:1为解答关键,注意掌握加成反应原理,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
13.下列化学方程式书写正确的是( )
| A. | 2P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O5 | B. | Fe2O3+3CO═2Fe+3CO2 | ||
| C. | H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2↑+O2↑ | D. | NaHCO3+HCl═NaCl+H2O+CO2↑ |
10.我国古代科技在造纸、印刷、纺织、陶瓷、冶铸、火药等方面都有引以为傲的发明创造.下列说法正确的是( )
| A. | 陶瓷的主要成分属于硅酸盐,硅酸盐与酸、碱都不反应 | |
| B. | 青铜铸造的器皿在空气中易发生析氢腐蚀,铜为原电池负极反应物 | |
| C. | 以树皮和麻绳为原料所造的纸张其主要成分是纤维素,纤维素与淀粉互为同分异构体 | |
| D. | 黑火药反应:2KNO3+S+3C═K2S+N2+3CO2 的还原剂只有C |
17.硫酸锌被广泛应用于医药领域和工农业生产.工业上由氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)生产ZnSO4•7H2O的一种流程如图:
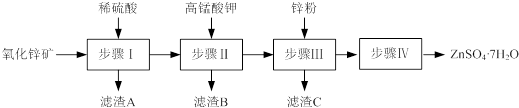
(1)步骤Ⅰ的操作是过滤,滤渣A的主要成分是H2SiO3.
(2)步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是H2SiO3+2NaOH=Na2SiO3+2H2O.
(3)步骤Ⅱ中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO(OH)2两种沉淀,该反应的离子方程式为3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+.
(4)步骤Ⅲ中,加入锌粉的作用是换出Cu,除去Cu2+.所得的滤液中含有的金属阳离子有Zn2+、K+.
(5)已知硫酸锌的溶解度与温度之间的关系如下表:
从硫酸锌溶液中获得硫酸锌晶体的实验操作为60℃条件下蒸发浓缩、降温结晶、过滤.
烘干操作需在减压低温条件下进行,原因是降低烘干的温度,防止ZnSO4•7H2O分解.
(6)取28.70g ZnSO4•7H2O加热至不同温度,剩余固体的质量变化如图所示.
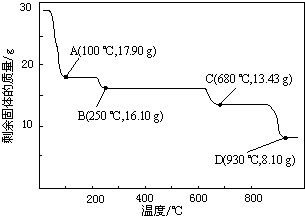
分析数据,680℃时所得固体的化学式为b.
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O.

(1)步骤Ⅰ的操作是过滤,滤渣A的主要成分是H2SiO3.
(2)步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是H2SiO3+2NaOH=Na2SiO3+2H2O.
(3)步骤Ⅱ中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO(OH)2两种沉淀,该反应的离子方程式为3Fe2++MnO4-+8H2O=3Fe(OH)3↓+MnO(OH)2↓+5H+.
(4)步骤Ⅲ中,加入锌粉的作用是换出Cu,除去Cu2+.所得的滤液中含有的金属阳离子有Zn2+、K+.
(5)已知硫酸锌的溶解度与温度之间的关系如下表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
烘干操作需在减压低温条件下进行,原因是降低烘干的温度,防止ZnSO4•7H2O分解.
(6)取28.70g ZnSO4•7H2O加热至不同温度,剩余固体的质量变化如图所示.

分析数据,680℃时所得固体的化学式为b.
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O.
7. 将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )
将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )
 将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )
将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述不正确的是( )| A. | O~A段反应的离子方程式是Ba2++CO32-═BaCO3↓ | |
| B. | A~B段反应的离子方程式是2OH-+CO2═CO${\;}_{3}^{2-}$+H2O | |
| C. | A~B段与C~D段所发生的反应相同 | |
| D. | D~E段沉淀的减少是由于碳酸钡固体与CO2的水溶液反应所致 |
11.下列过程或现象与盐类水解无关的是( )
| A. | 用热的纯碱溶液去油污 | B. | 硫酸氢钠溶液显酸性 | ||
| C. | 小苏打溶液显弱碱性 | D. | 浓硫化钠溶液有臭味 |
1.下列分子中δ键与π键数之比为3:1的是( )
| A. | N2 | B. | C2H4 | C. | HCHO | D. | HCN |