��Ŀ����
5����Ʒ������Ϊ������������������ҽҩ���ܼ����ϳ�a-��Ʒ��G��·��֮һ��ͼ��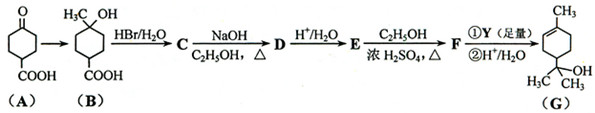
��֪��RCOOC2H5
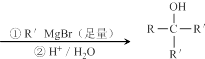
��ش��������⣺
��1��A���������ŵ��������ʻ����Ȼ���
��2��A���⻯��Z��C7H12O3����д��Z��һ�������¾ۺϷ�Ӧ�Ļ�ѧ����ʽ��
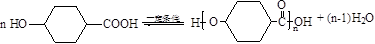 ��
����3��B�ķ���ʽΪC8H14O3��д��ͬʱ��������������B����״ͬ���칹��Ľṹ��ʽ��
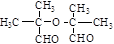 ��
���ٺ˴Ź���������2�����շ� ���ܷ���������Ӧ
��4��B��C��E��F�ķ�Ӧ���ͷֱ�Ϊȡ����Ӧ��ȡ����Ӧ��������Ӧ��
��5��C��D�Ļ�ѧ����ʽΪ
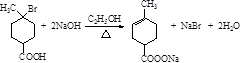 ��
��
���� ��A��B�Ľṹ��֪��A����鷢���ӳɷ�Ӧ����B��B��HBr����ȡ����Ӧ����CΪ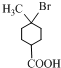 ��C������ȥ��Ӧ����DΪ
��C������ȥ��Ӧ����DΪ ��D�ữ�õ�EΪ
��D�ữ�õ�EΪ ��E���Ҵ�����������Ӧ����FΪ
��E���Ҵ�����������Ӧ����FΪ ��F������Ϣ��Ӧ����G�����F��G�Ľ�Ͽ�֪YΪCH3MgBr���ݴ˷������
��F������Ϣ��Ӧ����G�����F��G�Ľ�Ͽ�֪YΪCH3MgBr���ݴ˷������
��� �⣺��A��B�Ľṹ��֪��A����鷢���ӳɷ�Ӧ����B��B��HBr����ȡ����Ӧ����CΪ ��C������ȥ��Ӧ����DΪ
��C������ȥ��Ӧ����DΪ ��D�ữ�õ�EΪ
��D�ữ�õ�EΪ ��E���Ҵ�����������Ӧ����FΪ
��E���Ҵ�����������Ӧ����FΪ ��F������Ϣ��Ӧ����G�����F��G�Ľ�Ͽ�֪YΪCH3MgBr��
��F������Ϣ��Ӧ����G�����F��G�Ľ�Ͽ�֪YΪCH3MgBr��
��1��A�й�����Ϊ�ʻ����Ȼ����ʴ�Ϊ���ʻ����Ȼ���
��2��A���⻯��Z��C7H12O3����A����������Z�����Z�ķ���ʽ��֪���÷�ӦΪ�ʻ������������ӳɷ�Ӧ����ZΪ ��Zͨ��������Ӧ���е����۷�Ӧ���ɸ߾���÷�Ӧ����ʽΪ
��Zͨ��������Ӧ���е����۷�Ӧ���ɸ߾���÷�Ӧ����ʽΪ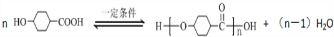 ��
��
�ʴ�Ϊ��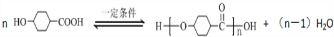 ��
��
��3��B�ķ���ʽΪC8H14O3��B����״ͬ���칹����������������ٺ˴Ź���������2�����շ壬˵������������ԭ�ӣ����ܷ���������Ӧ��˵������ȩ��������������Ľṹ��ʽΪ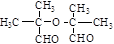 ��
��
�ʴ�Ϊ��C8H14O3��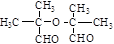 ��
��
��4����B��C�ķ�Ӧ������֪��B����ˮ�ⷴӦ���� ������ȡ����Ӧ��E��Fˮ�����봼������������Ӧ��ȡ����Ӧ��
������ȡ����Ӧ��E��Fˮ�����봼������������Ӧ��ȡ����Ӧ��
�ʴ�Ϊ��ȡ����Ӧ��������Ӧ��ȡ����Ӧ��
��5��C��D�Ļ�ѧ����ʽΪ 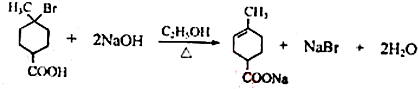 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ���ƶϼ�֪ʶ�ۺ�������������ȷ�����ż������ʹ�ϵ����Ӧ��������Ӧ�����ǽⱾ��ؼ���ע���л���Ӧ�жϼ��ͳɼ���ʽ���ѵ���ͬ���칹��ṹ��ʽȷ������Ŀ�Ѷ��еȣ�

| A�� | n-2m | B�� | 2m-n | C�� | 8+n-2m | D�� | 2m-n-8 |
| A�� | 2P+5O2$\frac{\underline{\;��ȼ\;}}{\;}$P2O5 | B�� | Fe2O3+3CO�T2Fe+3CO2 | ||
| C�� | H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2��+O2�� | D�� | NaHCO3+HCl�TNaCl+H2O+CO2�� |
| A�� | �մɵ���Ҫ�ɷ����ڹ����Σ����������ᡢ�����Ӧ | |
| B�� | ��ͭ����������ڿ������������ⸯʴ��ͭΪԭ��ظ�����Ӧ�� | |
| C�� | ����Ƥ������Ϊԭ�������ֽ������Ҫ�ɷ�����ά�أ���ά������ۻ�Ϊͬ���칹�� | |
| D�� | �ڻ�ҩ��Ӧ��2KNO3+S+3C�TK2S+N2+3CO2 �Ļ�ԭ��ֻ��C |
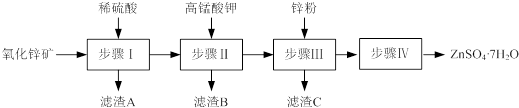
��1�������IJ����ǹ��ˣ�����A����Ҫ�ɷ���H2SiO3��
��2����������ϡ����������ʱ���費��ͨ�����ˮ������Ŀ����H2SiO3+2NaOH=Na2SiO3+2H2O��
��3��������У���pHԼΪ5.1����Һ�м��������أ�����Fe��OH��3��MnO��OH��2���ֳ������÷�Ӧ�����ӷ���ʽΪ3Fe2++MnO4-+8H2O=3Fe��OH��3��+MnO��OH��2��+5H+��
��4��������У�����п�۵������ǻ���Cu����ȥCu2+�����õ���Һ�к��еĽ�����������Zn2+��K+��
��5����֪����п���ܽ�����¶�֮��Ĺ�ϵ���±���
| �¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 |
| �ܽ��/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
��ɲ������ڼ�ѹ���������½��У�ԭ���ǽ��ͺ�ɵ��¶ȣ���ֹZnSO4•7H2O�ֽ⣮
��6��ȡ28.70g ZnSO4•7H2O��������ͬ�¶ȣ�ʣ�����������仯��ͼ��ʾ��
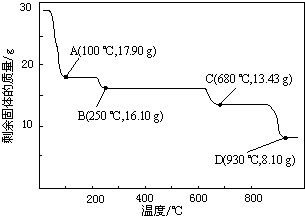
�������ݣ�680��ʱ���ù���Ļ�ѧʽΪb��
a��ZnO b��Zn3O��SO4��2 c��ZnSO4 d��ZnSO4•H2O��
| A�� | ʹpH��ֽ�ʺ�ɫ����Һ�У�I-��NO3-��SO42-��Na+ | |
| B�� | ˮ�������c��H+��=1��10-13mol/L����Һ�У�CO32-��K+��ClO-��SO32- | |
| C�� | ��$\frac{c��{H}^{+}��}{c��O{H}^{-}��}$=1��1012����Һ�У�NH4+��Ca2+��C1-��K+ | |
| D�� | ���������ܲ���������������Һ�У�NH4+��Na+��NO3-��SO42- |

 ��R=-CH3��-H��
��R=-CH3��-H�� $\stackrel{Fe/HCl}{��}$
$\stackrel{Fe/HCl}{��}$
 $\stackrel{KMnO_{4}/H+}{��}$
$\stackrel{KMnO_{4}/H+}{��}$
 ����A�ķ�Ӧ������ȡ����Ӧ��������Ӧ��
����A�ķ�Ӧ������ȡ����Ӧ��������Ӧ��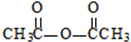 ��
��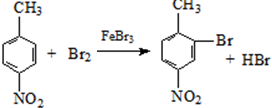 ��
��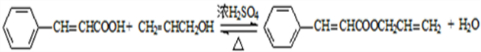 ��
�� ��д������һ�ֽṹ��ʽ����
��д������һ�ֽṹ��ʽ����
 ��
��