题目内容
19.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 常温下,46g NO2和N2O4含有2NA个氧原子 | |
| B. | 1mol Na中约含NA个电子 | |
| C. | 4gNaOH中含有NA个OH- | |
| D. | 标况下,22.4LHF中含有NA个HF分子 |
分析 A、NO2和N2O4的最简式均为NO2;
B、钠外围有11个电子;
C、4gNaOH的物质的量为0.1mol;
D、标况下,HF为液体.
解答 解:A、NO2和N2O4的最简式均为NO2,故46g混合气体中含有的NO2的物质的量n=$\frac{46g}{46g/mol}$=1mol,则由于2mol氧原子,即2NA个,故A正确;
B、钠外围有11个电子,所以1mol Na中约含11NA个电子,故B错误;
C、4gNaOH的物质的量为0.1mol,所以4gNaOH中含有0.1NA个OH-,故C错误;
D、标况下,HF为液体,不能根据气体摩尔体积来计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的应用,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.蒸干下列溶液能得到原溶液中溶质的是( )
| A. | AlCl3 | B. | Cu(NO3)2 | C. | FeSO4 | D. | Na2CO3 |
10.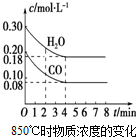 已知:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0
已知:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0
(1)在一体积为10L的密闭容器中,通入一定量的CO和H2O,在850℃时CO和H2O浓度变化如图,则0~4min的平均反应速率v(H2O)=0.03mol•(L•min)-1.
(2)t℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如表:
①若c1数值大于0.08mol•L-1,则温度t>850℃(填“>”“<”或“=”).
②表中3~4min之间反应处于平衡 状态.
③若第5min时,该反应处于化学平衡状态,则此反应的平衡常数K=0.35(保留两位有效数字)
④表中5~6min之间数值发生变化,可能的原因是B.
A.升高温度
B.体积不变,通入水蒸气
C.缩小体积,增大压强
D.体积不变,通入氢气
⑤比较反应物CO在2~3min、5~6min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)表示]的大小v(2~3)>v(5~6)(假设3~5min内反应条件不变).
⑥能使该反应的反应速率增大,且平衡向正反应方向移动的措施是C.
A.适当升高温度 B.缩小反应容器的体积C.增大CO的浓度 D.选择高效催化剂.
 已知:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0
已知:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0(1)在一体积为10L的密闭容器中,通入一定量的CO和H2O,在850℃时CO和H2O浓度变化如图,则0~4min的平均反应速率v(H2O)=0.03mol•(L•min)-1.
(2)t℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如表:
| 时间/min | c(CO)/mol•L-1 | c(H2O)/mol•L-1 | c(CO2)/mol•L-1 | c(H2)/mol•L-1 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.110 | 0.210 | 0.090 | |
| 6 | 0.096 | 0.266 | 0.104 |
②表中3~4min之间反应处于平衡 状态.
③若第5min时,该反应处于化学平衡状态,则此反应的平衡常数K=0.35(保留两位有效数字)
④表中5~6min之间数值发生变化,可能的原因是B.
A.升高温度
B.体积不变,通入水蒸气
C.缩小体积,增大压强
D.体积不变,通入氢气
⑤比较反应物CO在2~3min、5~6min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)表示]的大小v(2~3)>v(5~6)(假设3~5min内反应条件不变).
⑥能使该反应的反应速率增大,且平衡向正反应方向移动的措施是C.
A.适当升高温度 B.缩小反应容器的体积C.增大CO的浓度 D.选择高效催化剂.
7.在两个密闭容器中,分别充有质量相等的N2、O2两种气体,它们的温度和密度均相同.下列说法中正确的是( )
| A. | 分子数:N2<O2 | B. | 气体摩尔体积:N2<O2 | ||
| C. | 气体的压强:N2<O2 | D. | 体积:N2<O2 |
14.下列物质一定属于同系物的是( )
①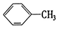 ②
②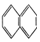 ③
③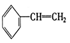 ④C2H4⑤CH2=CH-CH=CH2⑥C3H4⑦
④C2H4⑤CH2=CH-CH=CH2⑥C3H4⑦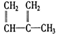 ⑧
⑧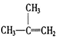
①
 ②
② ③
③ ④C2H4⑤CH2=CH-CH=CH2⑥C3H4⑦
④C2H4⑤CH2=CH-CH=CH2⑥C3H4⑦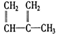 ⑧
⑧
| A. | ④和⑥ | B. | ①、②和③ | C. | ⑤和⑦ | D. | ④、⑥和⑧ |
8.有转化关系(其他产物及反应所需条件均已略去).A$\stackrel{X}{→}$B$\stackrel{Cl_{2}}{→}$C$\stackrel{O_{2}}{→}$D$\stackrel{O_{2}}{→}$E$\stackrel{H_{2}O}{→}$F,以下推断错误的是( )
| A. | 当X是盐酸时,则F是稀硝酸24 | |
| B. | 当X是氢氧化钠时,则F是稀硝酸y | |
| C. | 当X是氢氧化钠时,B跟Cl2反应可能有白烟现象e | |
| D. | 当X是氢氧化钠时,B能使酸性高锰酸钾溶液褪色N |
9.下列说法正确的是( )
| A. | 热化学方程式中,如没有注明温度和压强,表示反应热是在标准状况下测得的数据 | |
| B. | 物质发生化学变化不一定伴随着能量变化 | |
| C. | 发生碰撞的分子只要具有足够的能量,就能够发生有效碰撞 | |
| D. | 化学反应速率可通过实验测定,比如可以测量在一定温度和压强下释放出的气体的体积,或者可以用比色的方法测定溶液颜色的深浅进行换算 |
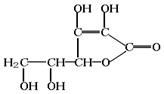
 ,其中氮的化合价为-2.
,其中氮的化合价为-2.