题目内容
9.下列关于化学键的说法正确的是( )| A. | 含有金属元素的化合物一定是离子化合物 | |
| B. | 第ⅠA族和第ⅦA族原子化合时,一定生成离子键 | |
| C. | 由非金属元素形成的化合物一定不是离子化合物 | |
| D. | 离子化合物中可能同时含有离子键和共价键 |
分析 A、含有金属元素的化合物不一定是离子化合物;
B、第ⅠA族和第ⅦA族原子化合时,不一定生成离子键;
C、由非金属元素形成的化合物可能是离子化合物;
D、离子化合物中可能同时含有离子键和共价键.
解答 解:A、含有金属元素的化合物不一定是离子化合物,如氯化铝是共价化合物,故A错误;
B、第ⅠA族和第ⅦA族原子化合时,不一定生成离子键,可能生成共价键,如H元素和F元素能形成共价化合物HF,故B错误;
C、由非金属元素形成的化合物可能是离子化合物,如铵盐,故C错误;
D、离子化合物中可能同时含有离子键和共价键,如NaOH,故D正确;
故选D.
点评 本题考查了化合物和化学键的关系,明确物质的构成微粒及微粒间的作用力即可解答,注意不能根据是否含有金属元素判断离子键,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列说法正确的是( )
| A. | 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 | |
| B. | 物质发生化学变化一定伴随着能量变化,且能量形式只表现为热量变化 | |
| C. | 把石墨完全转化为金刚石时,要吸收能量,所以石墨不如金刚石稳定 | |
| D. | 原子结合成分子的过程一定释放出能量 |
14.要增大铁与盐酸反应的速率,所采取的下列措施中无效的是( )
| A. | 增大盐酸的浓度 | B. | 增大压强 | C. | 提高反应的温度 | D. | 用铁粉代替铁片 |
1.下列属于吸热反应的是( )
| A. | 镁的燃烧反应 | B. | 盐酸与氢氧化钠的反应 | ||
| C. | 水的分解反应 | D. | 铝与盐酸的反应 |
18.下列有关说法正确的是( )
| A. | 氨水稀释后,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值减小 | |
| B. | 0.1 mol•L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 | |
| C. | 298 K时,2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行,则其△H<0 | |
| D. | 对N2(g)+3H2(g)═2NH3(g),其他条件不变时充入N2,正反应速率增大,逆反应速率减小 |
1.建构数学模型来研究化学问题,既直观又简洁.下列建构的数轴模型正确的是( )
| A. | 钠在氧气中燃烧,钠的氧化产物: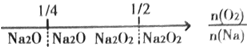 | |
| B. | 铁在Cl2中燃烧,铁的氧化产物: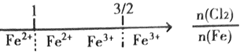 | |
| C. | A1Cl3溶液中滴加NaOH溶液后体系中铝元素的存在形式: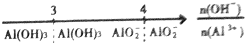 | |
| D. | FeI2溶液中通入Cl2,铁元素存在形式: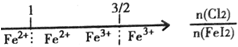 |