题目内容
19.等质量的两份锌粉a、b,分别加入过量的稀硫酸,同时向a中加入少量的CuSO4溶液,如图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )| A. |  | B. | 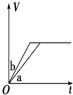 | C. | 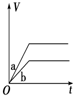 | D. | 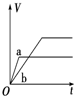 |
分析 锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加速金属锌和硫酸反应的速率,产生氢气的量取决于金属锌的质量.
解答 解:锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加速金属铁和硫酸反应的速率,所以反应速率是:a>b,速率越大,锌完全反应时所用的时间越短,所以a所用的时间小于b的时间;产生氢气的量取决于金属锌的质量,而a中,金属锌一部分用于置换金属铜,导致和硫酸反应生成氢气的量减少,所以氢气的体积是:a<b.
故选D.
点评 本题考查了根据图象判断反应速率的大小,难度不大,分析图象时注意图象中坐标的含义、拐点变化趋势来解答.

练习册系列答案
 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
9.某有机物A在酸性溶液中加热可发生如下反应,下列说法错误的是( )
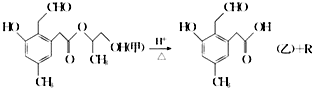

| A. | R为二元醇,不能发生银镜反应 | |
| B. | 1 mol甲在一定条件下与氢气反应,最多可消耗 5mol H2 | |
| C. | 甲在碱性条件下也可发生水解反应 | |
| D. | 甲和乙均能发生银镜反应 |
10.为探究溴乙烷与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙两位同学分别设计如下实验方案:
甲:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应.
乙:向反应混合液中滴入硝酸中和NaOH,然后再滴入AgNO3溶液,若有浅黄色沉淀生成,则可证明发生了消去反应.
则有关上述实验方案的叙述正确的是( )
甲:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应.
乙:向反应混合液中滴入硝酸中和NaOH,然后再滴入AgNO3溶液,若有浅黄色沉淀生成,则可证明发生了消去反应.
则有关上述实验方案的叙述正确的是( )
| A. | 甲正确 | B. | 乙正确 | C. | 甲、乙均正确 | D. | 甲、乙均不正确 |
7.下列关于能量转换的认识不正确的是( )
| A. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| B. | 白炽灯工作时,电能全部转化为光能 | |
| C. | 煤燃烧时,化学能主要转化为热能 | |
| D. | 绿色植物的光合作用时,将光能转变为化学能 |
4.下列涉及有机物的说法正确的是( )
| A. | 2-己烯能使KMnO4(H+)溶液褪色 | |
| B. | 汽油、煤油、柴油和植物油都是碳氢化合物 | |
| C. | 乙烯、苯都可与溴水发生加成反应 | |
| D. | 乙烯和聚乙烯都能发生加聚反应 |
11.下列有关化学用语表示正确的是( )
| A. | 次氯酸的电子式 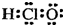 | |
| B. | S2-的结构示意图: | |
| C. | 质子数为92,中子数为143的铀原子:23592U | |
| D. | NH4I的电子式: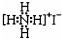 |
8.下列实验装置能达到实验目的是(夹持仪器未画出)( )
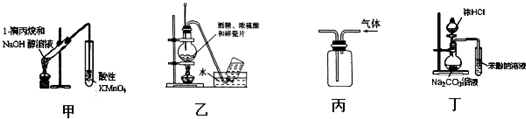

| A. | 用甲装置检验1-溴丙烷消去产物 | |
| B. | 实验室用乙装置制取乙烯 | |
| C. | 用丙装置收集甲烷气体 | |
| D. | 用丁装置证明酸性强弱:盐酸>碳酸>苯酚 |
9.下列关于化学键的说法正确的是( )
| A. | 含有金属元素的化合物一定是离子化合物 | |
| B. | 第ⅠA族和第ⅦA族原子化合时,一定生成离子键 | |
| C. | 由非金属元素形成的化合物一定不是离子化合物 | |
| D. | 离子化合物中可能同时含有离子键和共价键 |