题目内容
14.下列说法错误的是( )| A. | 酚类化合物有毒,不能用于杀菌消毒 | |
| B. | 乙烯可催熟水果 | |
| C. | 石油的裂解可获得乙烯、丙烯等短链烯烃 | |
| D. | 甲醛的水溶液可用于防腐 |
分析 A.苯酚可以用于杀菌消毒;
B.乙烯为植物生长调节剂;
C.裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯等;
D.福尔马林可用于防腐.
解答 解:A.苯酚可以用于杀菌消毒,故A错误;
B.乙烯为植物生长调节剂,可用作水果催熟剂,故B正确;
C.石油的裂解可获得乙烯、丙烯、丁二烯、丁烯等短链烯烃,故C正确;
D.甲醛的水溶液称为福尔马林,用于防腐,故D正确;
故选A.
点评 本题考查苯酚、乙烯、甲醛的用途、石油加工等,侧重于常识性内容的考查,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
4.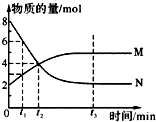 在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
 在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )| A. | 反应的化学方程式为:2M?N | B. | t2时,正逆反应速率相等 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t1时,N的浓度是M浓度的2倍 |
5.最近美国宇航局(NASA)马里诺娃博士找到了一种比CO2有效104倍的“超级温室气体”--全氟丙烷(C3F8),并提出用其“温室化火星”,使火星成为第二个地球的计划.有关全氟丙烷的说法正确的是( )
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的结构式为 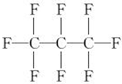 | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 全氟丙烷分子中只有极性键 |
2.含有共价键的离子化合物是( )
| A. | KCl | B. | HF | C. | NaOH | D. | CaCl2 |
19.研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题:
(1)C、Si、N的电负性由大到小的顺序是N>C>Si.C60和金刚石都是碳的同素异形体,二者比较,熔点高的是金刚石.
(2)A、B均为短周期金属元素,依据如表数据,写出B的基态原子的电子排布式1S22S22P63S2.
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色.如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+有(填“无”或“有”)颜色.
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.
①每个COCl2分子内含有3个σ键,1个π键.其中心原子采取SP2杂化轨道方式.
②配合物Fe(CO)5的配体是CO.
(1)C、Si、N的电负性由大到小的顺序是N>C>Si.C60和金刚石都是碳的同素异形体,二者比较,熔点高的是金刚石.
(2)A、B均为短周期金属元素,依据如表数据,写出B的基态原子的电子排布式1S22S22P63S2.
| 电离能 /(kJ•mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.
①每个COCl2分子内含有3个σ键,1个π键.其中心原子采取SP2杂化轨道方式.
②配合物Fe(CO)5的配体是CO.
6.对于达到平衡状态的可逆反应:N2+3H2?2NH3,下列有关叙述正确的是( )
| A. | N2和NH3的质量分数相等 | |
| B. | N2、H2、NH3的浓度之比为1:3:2 | |
| C. | 当断开1mol氮氮三键的同时,断开3mol氢氢键 | |
| D. | 氮气的体积分数保持不变 |
3.W是由短周期元素X、Y、Z组成的盐.X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍;X、Y原子最外层电子数之和等于Z原子的最外层电子数;Y、Z同周期且相邻,但与X不同周期.下列说法一定正确的是( )
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | W晶体中只存在有共价键 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
4.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 标准状况下,33.6 L SO3分子含有的硫原子数为1.5NA | |
| B. | 1 mol/L KI溶液中I-数目为NA | |
| C. | 0.1 mol Na+离子中所含的电子数为3.4 NA | |
| D. | 56g铁与足量的Cl2或S反应时转移电子数均为3 NA |
 ;元素Z的离子结构示意图为
;元素Z的离子结构示意图为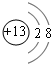 .
.