题目内容
17.下列说法正确的是(设NA为阿伏加德罗常数)( )| A. | 常温常压下,28g氮气的体积约为22.4升 | |
| B. | 标准状况下,11.2L水含有1mol氢原子 | |
| C. | 标准状况下,11.2L氧气与硫充分反应,转移的电子数目为2NA | |
| D. | 常温常压下,1mol氯气完全被碱吸收需要NA个氢氧根离子 |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、标况下水为液态;
C、求出氧气的物质的量,然后根据氧气和硫反应后变为-2价来分析;
D、氯气和碱的反应为:Cl2+2OH-=Cl-+ClO-+H2O.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故28g氮气的物质的量为1mol,则体积大于22.4L,故A错误;
B、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量和含有的H原子个数,故B错误;
C、标况下11.2L氧气的物质的量为0.5mol,而氧气和硫反应后变为-2价,故0.5mol氧气转移2NA个电子,故C正确;
D、氯气和碱的反应为:Cl2+2OH-=Cl-+ClO-+H2O,故1mol氯气完全被碱吸收需要2NA个氢氧根,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
7.被称为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在另一边镀二氧化锰.在纸内是离子“流过”水和氧化锌组成的电解液.电池总反应Zn+2MnO2+H2O═ZnO+2MnO(OH),下列说法正确的是( )
| A. | 该电池的电流方向是由锌到二氧化猛 | |
| B. | 该电池反应中MnO2起催化作用 | |
| C. | 当0.1molZn完全溶解时,流经电解液的电子个数为1.204×1023 | |
| D. | 电池正极反应为MnO2+e-+H2O═MnO(OH)+OH- |
5.下列说法正确的是( )
| A. | 根据能量守恒定律,反应物能量之和等于生成物能量之和 | |
| B. | 化学反应一定伴随能量变化,有能量变化也一定伴随化学反应 | |
| C. | 反应物所具有的总能量比生成物所具有的总能量高的反应是放热反应 | |
| D. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
12.动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等.
仪器:①酒精灯,试管,烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和②③的化学方程式)
写出下列实验步骤所对应的化学方程式②Na2S+Cl2=2NaCl+S,③2Na+2H2O=2NaOH+H2↑,
(4)实验结论:同周期元素从左往右失电子能力逐渐减弱,得电子能力逐渐增强.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭. |
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等.
仪器:①酒精灯,试管,烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和②③的化学方程式)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
(4)实验结论:同周期元素从左往右失电子能力逐渐减弱,得电子能力逐渐增强.
2.下列物质①Cl2 ②盐酸 ③氯水 ④盐酸酸化的漂白粉溶液 ⑤过氧化钠 ⑥木炭能使紫色石蕊试液由紫变红又褪色的是( )
| A. | ①②③④ | B. | ①③④⑤ | C. | ②③④⑥ | D. | ①③④ |
6.对于实验I~IV的实验现象预测正确的是( )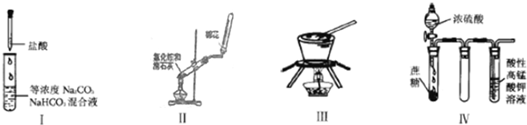

| A. | 实验I:逐滴滴加盐酸时,试管中立即产生大量气泡 | |
| B. | 实验II:实验室制取并收集氨气 | |
| C. | 实验III:从饱和食盐水中提取NaCl晶体 | |
| D. | 装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅直至褪去 |
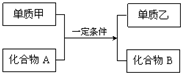 置换反应的通式可用如图表示,单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
置换反应的通式可用如图表示,单质甲、乙和化合物A、B为中学常见物质,请回答下列问题: