题目内容
5.下列说法正确的是( )| A. | 根据能量守恒定律,反应物能量之和等于生成物能量之和 | |
| B. | 化学反应一定伴随能量变化,有能量变化也一定伴随化学反应 | |
| C. | 反应物所具有的总能量比生成物所具有的总能量高的反应是放热反应 | |
| D. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
分析 A、化学反应一定伴随能量变化,化学反应的总能量守恒;
B、化学反应一定伴随能量变化,有能量变化不一定伴随化学反应;
C、放热反应中反应物所具有的总能量比生成物所具有的总能量高;
D、固体硫转化为气体硫属于吸热的过程,物质的燃烧是放热的过程.
解答 解:A、化学反应一定伴随能量变化,化学反应的总能量守恒,反应物能量之和一定不等于生成物能量之和,故A错误;
B、化学反应一定伴随能量变化,有能量变化不一定伴随化学反应,如固体的溶解过程放热,属于物理变化过程,故B错误;
C、放热反应中反应物所具有的总能量比生成物所具有的总能量高,吸热反应中反应物所具有的总能量比生成物所具有的总能量低,故C正确;
D、固体硫转化为气体硫属于吸热的过程,物质的燃烧是放热的过程,质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多,故D错误.
故选C.
点评 本题考查学生化学反应中的能量转化知识,属于基本知识的考查,难度不大.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
18.用下列三种装置制备和收集二氧化碳气体:

将收集的三瓶CO2置于天平上称量,若三个集气瓶的体积与质量均相等,称量结果正确的是( )

将收集的三瓶CO2置于天平上称量,若三个集气瓶的体积与质量均相等,称量结果正确的是( )
| A. | ①最重 | B. | ②最重 | C. | ③最重 | D. | ①②③一样重 |
16.有一包铁粉和铜粉混合均匀的粉末样品,为确定其组成,某同学将不同质量的该样品分别与40mL 1mol/L的FeCl3溶液反应,实验结果如表所示(忽略反应前后溶液体积的微小变化).
下列实验结论不正确的是( )
| 实验序号 | ① | ② | ③ | ④ |
| m(粉末样品)/g | 0.90 | 1.80 | 3.60 | 7.20 |
| m(反应后剩余固体)/g | 0 | 0.64 | 2.48 | 6.08 |
| A. | 实验①反应后溶液中含有Fe3+、Fe2+、Cu2+ | |
| B. | 实验②③反应后剩余固体全部是Cu | |
| C. | 实验④的滤液中c(Fe2+)=1.5 mol/L | |
| D. | 原粉末样品中m(Fe):m(Cu)=7:8 |
17.下列说法正确的是(设NA为阿伏加德罗常数)( )
| A. | 常温常压下,28g氮气的体积约为22.4升 | |
| B. | 标准状况下,11.2L水含有1mol氢原子 | |
| C. | 标准状况下,11.2L氧气与硫充分反应,转移的电子数目为2NA | |
| D. | 常温常压下,1mol氯气完全被碱吸收需要NA个氢氧根离子 |
14.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 标准状况下,2.24 L H2O中所含的原子总数为0.3NA | |
| B. | 0.1 molCl2与足量的NaOH稀溶液反应,转移的电子总数为0.2NA | |
| C. | 1mol•L一1的NaCl溶液中所含Na+数目为NA | |
| D. | 常温常压下,14g由N2和CO组成的混合气体中含有的原子总数为NA |
15.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
| 物质 | 试剂 | 分离方法 | |
| ① | 氯化钠(硝酸钾) | 蒸馏水 | 降温结晶 |
| ② | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(苯酚) | 浓溴水 | 分液 |
| A. | ②③ | B. | ①③ | C. | 只有③ | D. | ③④ |
 根据如图反应框图填空.已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.
根据如图反应框图填空.已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.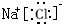
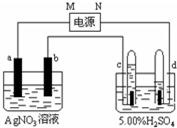 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.试管充满水,通电一段时间后,在c、d两极上共收集到标准状态下336mL气体,体积如图所示.请回答下列问题.
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.试管充满水,通电一段时间后,在c、d两极上共收集到标准状态下336mL气体,体积如图所示.请回答下列问题.