题目内容
1.元素在周期表中的位置反映了元素的性质.第3周期元素中,原子半径最大的是( )| A. | Na | B. | Si | C. | S | D. | Cl |
分析 同一周期的元素从左到右电子层数相同,而核电荷数逐渐增多,据此分析原子半径变化规律.
解答 解:同一周期的元素从左到右电子层数相同,而核电荷数逐渐增多,故原子核对核外电子层的吸引力逐渐增大,故原子半径逐渐减小,而第三周期的元素从左到右为:Na、Mg、Al、Si、P、S、Cl,故原子半径最大的为Na,故选A.
点评 本题考查了同周期的原子半径大小比较,难度不大,应注意掌握影响原子半径大小的因素.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
11. 回答下列问题:
回答下列问题:
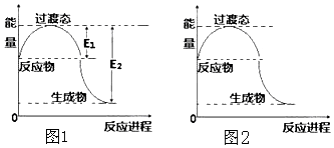
(1)2molCH4(g)和4mol O2(g)反应生成CO2(g)和H2O(g)过程中的能量变化如图1所示.已知E1=134KJ,E2=368KJ.则热化学方程式为2CH4(g)+4O2(g)=2CO2(g)+4H2O(g)△H=-234 kJ•mol-1生成18g H2O(l)放出或吸收的能量(范围)>58.5KJ
请在图2中画出加入催化剂后,反应过程中的能量变化曲线.
(2)在一定条件下,已知下列反应的热化学反应式:
C(石墨,s)+O2(g)=CO2(g)△H1; 2H2(g)+O2(g)=2H2O(l)△H2
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3
由C(石墨,s)和气态H2反应合成气态1mol C2H2的热化学方程式2C (s,石墨)+H2(g)=C2H2(g))△H=2△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3;
(3)工业上可通过CO(C≡O)和H2化合制得CH3OH(气态),各键能数据如表所示
写出合成1mol CH3OH(气态)的热化学方程式CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1.
 回答下列问题:
回答下列问题:(1)2molCH4(g)和4mol O2(g)反应生成CO2(g)和H2O(g)过程中的能量变化如图1所示.已知E1=134KJ,E2=368KJ.则热化学方程式为2CH4(g)+4O2(g)=2CO2(g)+4H2O(g)△H=-234 kJ•mol-1生成18g H2O(l)放出或吸收的能量(范围)>58.5KJ
请在图2中画出加入催化剂后,反应过程中的能量变化曲线.
(2)在一定条件下,已知下列反应的热化学反应式:
C(石墨,s)+O2(g)=CO2(g)△H1; 2H2(g)+O2(g)=2H2O(l)△H2
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3
由C(石墨,s)和气态H2反应合成气态1mol C2H2的热化学方程式2C (s,石墨)+H2(g)=C2H2(g))△H=2△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3;
(3)工业上可通过CO(C≡O)和H2化合制得CH3OH(气态),各键能数据如表所示
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能(kJ/mol) | 348 | 413 | 436 | 358 | 1072 | 463 |
12.某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用:
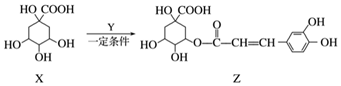
下列有关叙述中不正确的是( )

下列有关叙述中不正确的是( )
| A. | Z结构中有1个手性碳原子 | |
| B. | Y的分子式为C9H8O4 | |
| C. | 1 mol Z与足量NaOH溶液反应,最多消耗8 mol NaOH | |
| D. | Z与浓溴水既能发生取代反应又能发生加成反应 |
16.在2L0.1mol•L-1 Na2SO4溶液中,下列说法正确的是( )
| A. | Na+物质的量为0.2mol | B. | Na+物质的量浓度为0.2 mol•L-1 | ||
| C. | SO42-物质的量为0.1mol | D. | SO42-物质的量浓度为0.2 mol•L-1 |
6.一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+B(g)?2C(g)+D(s)已达到平衡状态的是( )
①混合气体的压强
②混合气体的密度
③B的物质的量浓度
④混合气体总物质的量
⑤混合气体的平均相对分子质量
⑥混合气体的总质量
⑦混合气体的总体积.
①混合气体的压强
②混合气体的密度
③B的物质的量浓度
④混合气体总物质的量
⑤混合气体的平均相对分子质量
⑥混合气体的总质量
⑦混合气体的总体积.
| A. | ②③⑤⑥ | B. | ①②③⑤⑥ | C. | ①②③⑤⑦ | D. | ②③④⑤ |
13.在任何条件下,纯水显中性,是因为( )
| A. | PH=7 | B. | c(H+)=c(OH-) | ||
| C. | c(H+)=c(OH-)=10-7mol/L | D. | c(H+)•c(OH-)=10-14 |
10.可用于鉴别以下三种化合物的一组试剂是( )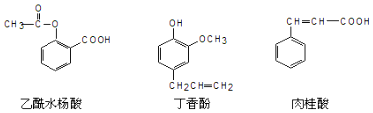
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液.

①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液.
| A. | ②与③ | B. | ③与④ | C. | ①与④ | D. | ①与② |
11.根据对角线规则,下列物质的性质具有相似性的是( )
| A. | 硼和硅 | B. | 铝和铁 | C. | 碳和铝 | D. | 铜和金 |