题目内容
10.可用于鉴别以下三种化合物的一组试剂是( )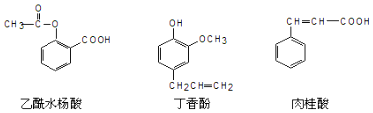
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液.
| A. | ②与③ | B. | ③与④ | C. | ①与④ | D. | ①与② |
分析 乙酰水杨酸中含有酯基和羧基,丁香酚中含有酚羟基和C=C,肉桂酸中含有C=C和羧基,可根据官能团的异同判断性质的移动,进而选择实验方法.
解答 解:乙酰水杨酸中含有酯基和羧基,丁香酚中含有酚羟基和C=C,肉桂酸中含有C=C和羧基,可加入溴的四氯化碳溶液,以鉴别乙酰水杨酸(不含C=C,不能使溴的四氯化碳溶液褪色),然后加入氯化铁溶液,可鉴别丁香酚,
故选A.
点评 本题考查有机物的鉴别,为高考常见题型,侧重考查学生的分析能力和实验能力,题目难度不大,本题注意把握有机物的官能团的性质,为解答该类题目的关键.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
1.元素在周期表中的位置反映了元素的性质.第3周期元素中,原子半径最大的是( )
| A. | Na | B. | Si | C. | S | D. | Cl |
18.下列实验设计正确的是( )
| A. | 将SO2通入溴水中证明SO2具有漂白性 | |
| B. | 将铁屑放入稀HNO3中证明Fe比H2活泼 | |
| C. | 将澄清石灰水中滴入某溶液后生成沉淀,说明滴入的溶液中含大量CO${\;}_{3}^{2-}$ | |
| D. | 石英砂可用于生产单晶硅 |
5.一定条件下的可逆反应2NO2 (红棕色)?2NO (无色)+O2 (无色),在恒压密闭容器充入NO2,达到化学平衡状态的标志是( )
| A. | 反应停止了 | |
| B. | NO的正反应速率与O2的逆反应速率相等 | |
| C. | c(NO):c(O2)=2:1 | |
| D. | 气体的颜色不再变化 |
15.设NA表示阿伏加德罗常数的值,下列叙述中对应的值为 NA的是( )
| A. | 30 g由乙酸和乳酸组成的混合物中所含有的O原子数 | |
| B. | Cu和足量的稀硝酸反应产生7.47 L NO气体时转移的电子数 | |
| C. | 0.25 mol丁烷中含有的非极性键数 | |
| D. | 1 mol FeCl3加入沸水制得的胶体中含有胶体粒子数 |
2.下列关于晶体的说法,不正确的是( )
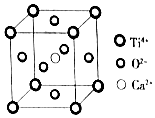
( Ti4+位于顶点上,O2-位于面心上,Ca2+位于中心)

( Ti4+位于顶点上,O2-位于面心上,Ca2+位于中心)
| A. | 该晶体的化学式为CaTiO3 | |
| B. | 该晶体中每个Ti4+和8个O2-相紧邻 | |
| C. | 一个CO2晶胞中平均含有4个CO2分子 | |
| D. | 金属晶体的熔点可能比分子晶体的熔点低 |
19.某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10mL 2mol•L-1稀硫酸,再插入一支温度计,温度计的温度由20℃逐渐升至35℃,随后,温度逐渐下降至30℃,最终停留在20℃.
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10mL 2mol•L-1硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来.
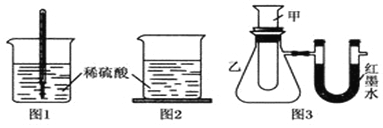
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应.
根据上述实验回答相关问题:
(1)方案一中,温度先升高的原因是铝和硫酸反应放出的热量使烧杯里溶液的温度升高,
升至最大值后又逐渐下降的原因是反应完全后,热量向空气中传递,烧杯里物质的温度降低.
(2)方案二中,小木片脱落的原因是氢氧化钠与硫酸的反应放热.
(3)由方案三的现象得出结论:①③④组物质发生的反应都是放热(填“吸热”或“放热”)反应.
(4)方案三实验②的U形管中的现象为红墨水液面左高右低,说明反应物的总能量小于(填“大于”“小于”或“等于”)生成物的总能量.
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10mL 2mol•L-1稀硫酸,再插入一支温度计,温度计的温度由20℃逐渐升至35℃,随后,温度逐渐下降至30℃,最终停留在20℃.
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10mL 2mol•L-1硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来.

方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应.
| 序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
| ① | 氧化钙与水 | 左低右高 |
| ② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
| ③ | 铝片与烧碱溶液 | 左低右高 |
| ④ | 铜与浓硝酸 | 左低右高 |
(1)方案一中,温度先升高的原因是铝和硫酸反应放出的热量使烧杯里溶液的温度升高,
升至最大值后又逐渐下降的原因是反应完全后,热量向空气中传递,烧杯里物质的温度降低.
(2)方案二中,小木片脱落的原因是氢氧化钠与硫酸的反应放热.
(3)由方案三的现象得出结论:①③④组物质发生的反应都是放热(填“吸热”或“放热”)反应.
(4)方案三实验②的U形管中的现象为红墨水液面左高右低,说明反应物的总能量小于(填“大于”“小于”或“等于”)生成物的总能量.
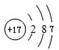 ;D微粒的核外电子排布式为1s2 2s22p6 3s23p6.
;D微粒的核外电子排布式为1s2 2s22p6 3s23p6.