题目内容
12.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 加入Mg能放出H2的溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 存在较多的Fe3+的溶液中:HCO3-、Cl-、SO42- | |
| C. | 水电离产生的c(OH-)=1×10-10 mol/L的溶液中:Al3+、SO42-、NO3-、Cl- | |
| D. | 使甲基橙变红色的溶液中:Na+、AlO2-、NO3-、CO32- |
分析 A.加入Mg能放出H2的溶液,显酸性;
B.离子之间相互促进水解;
C.水电离产生的c(OH-)=1×10-10 mol/L的溶液,为酸或碱溶液;
D.使甲基橙变红色的溶液,显酸性.
解答 解:A.加入Mg能放出H2的溶液,显酸性,该组离子之间不反应,可大量共存,故A正确;
B.Fe3+、HCO3-相互促进水解,不能大量共存,故B错误;
C.水电离产生的c(OH-)=1×10-10 mol/L的溶液,为酸或碱溶液,碱溶液中不能大量存在Al3+,故C错误;
D.使甲基橙变红色的溶液,显酸性,不能大量存在AlO2-、CO32-,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重水解反应、复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
20.实现下列变化时,需克服相同类型作用力的是( )
| A. | 二氧化硅和干冰的熔化 | B. | 液溴和液汞的气化 | ||
| C. | 食盐和冰的熔化 | D. | 纯碱和烧碱的熔化 |
4.下列物质碱性最强的是( )
| A. | LiOH | B. | KOH | C. | RbOH | D. | NaOH |
1.恒温下,在一密闭容器中,N2(g)+3H2(g)?2NH3(g)达到平衡后,测得c(H2)=2mol•L-1,N2的体积分数为20%,下列有关说法中正确的是( )
| A. | 将容器容积压缩一半,平衡向右移动,达到新平衡时c(H2)<2mol•L-1 | |
| B. | 向容器中加入0.1molN2,平衡向右移动,达到新平衡时N2的体积分数小于20% | |
| C. | 若达到新平衡时c(H2)=2.5mol•L-1,则改变的条件可能是降温或加压 | |
| D. | 若改变条件后,H2的百分含量增大,则平衡一定向逆反应方向移动 |
18.下列实验装置不能达到实验目的是( )
| A. |  用SO2做喷泉实验 | B. |  验证CU与浓HNO3反应的热量变化 | ||
| C. |  验证氨气易溶于水 | D. |  比较Na2CO3与NaHCO3的稳定性 |

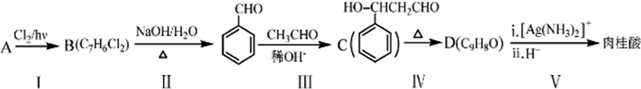

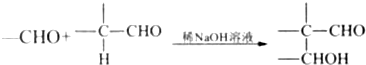
 .
. .肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是
.肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是 .
.