题目内容
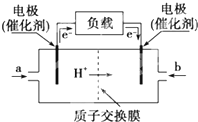 如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列有关该电池的说法错误的是( )
如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列有关该电池的说法错误的是( )| A、右边的电极为电池的负极,b处通入的是空气 |
| B、左边的电极为电池的负极,a处通入的是甲醇 |
| C、电池负极的反应式为:2CH3OH+2H2O-12e-═2CO2↑+12H+ |
| D、电池正极的反应式为:3O2+12H++12e-═6H2O |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、依据图中电子流向分析,原电池中电子是从负极流向正极;电子流出的一端是负极,流入的一端为正极,得到电子发生还原反应;
B、依据图中电子流向分析,原电池中电子是从负极流向正极;电子流出的一端是负极,失电子发生氧化反应;
C、负极是甲醇失电子发生氧化反应,依据电极反应的产物和环境写出电极反应式;
D、正极是氧气得到电子发生还原反应,氧气得到电子生成氢氧根离子,在图中是酸性介质,电极反应产物应写成水的形式.
B、依据图中电子流向分析,原电池中电子是从负极流向正极;电子流出的一端是负极,失电子发生氧化反应;
C、负极是甲醇失电子发生氧化反应,依据电极反应的产物和环境写出电极反应式;
D、正极是氧气得到电子发生还原反应,氧气得到电子生成氢氧根离子,在图中是酸性介质,电极反应产物应写成水的形式.
解答:
解:A、根据原电池中电子以及氢离子的移动方向,可知b为正极,正极上通入空气,故A错误;
B、依据图中电子流向分析,原电池中电子是从负极流向正极;电子流出的一端是负极,失电子发生氧化反应;所以a处是失电子的一端,通的是甲醇,故B正确;
C、负极是甲醇失电子发生氧化反应,依据电池反应和酸性环境,2CH3OH+3O2=2CO2+4H2O,负极电极反应为:CH3OH+H2O-6e-=CO2+6H+,故C正确;
D、正极是氧气得到电子发生还原反应,氧气得到电子生成氢氧根离子,在图中是酸性介质,电极反应产物应写成水的形式;电池的正极反应式为:O2+4H++4e-=2H2O,故D正确;
故选A.
B、依据图中电子流向分析,原电池中电子是从负极流向正极;电子流出的一端是负极,失电子发生氧化反应;所以a处是失电子的一端,通的是甲醇,故B正确;
C、负极是甲醇失电子发生氧化反应,依据电池反应和酸性环境,2CH3OH+3O2=2CO2+4H2O,负极电极反应为:CH3OH+H2O-6e-=CO2+6H+,故C正确;
D、正极是氧气得到电子发生还原反应,氧气得到电子生成氢氧根离子,在图中是酸性介质,电极反应产物应写成水的形式;电池的正极反应式为:O2+4H++4e-=2H2O,故D正确;
故选A.
点评:本题考查了原电池的原理应用,电极判断,电极名称,电极反应,电极反应式书写的分析判断,掌握原电池原理是解题关键,燃料电池的特征是燃料是电子在负极反应,氧气再正极发生还原反应,题目难度中等.

练习册系列答案
相关题目
在恒温、恒容的条件下,有反应2A(g)+2B(g)?C(g)+3D(g),现从两条途径分别建立平衡.途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L.则以下叙述不正确的是( )
| A、两途径最终达到平衡时,体系内混合气的平均相对分子质量不同 | ||
| B、两途径最终达到平衡时,体系内混合气的百分组成相同 | ||
| C、达平衡时,途径Ⅰ的反应速率v(A)小于途径Ⅱ的反应速率v(A) | ||
D、达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的
|
在标准状况下,进行甲、乙、丙三组实验:三组各取60mL同浓度盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
则下列说法正确的是( )
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A、甲组和乙组的实验中,盐酸均是过量的 |
| B、盐酸的物质的量浓度为0.8mol/L |
| C、合金中镁铝的物质的量之比为1:1 |
| D、丙组中铝的物质的量为0.018mol |
组成金属单质的微粒( )
| A、金属原子 |
| B、金属阳离子和电子 |
| C、金属原子和电子 |
| D、阳离子和阴离子 |
将2mol A和1mol B充入某密闭容器中发生反应:2A(g)+B(g)?xC(g),达到化学平衡后,C的体积分数为a.假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是(双选)( )
| A、若在恒温恒压下,当x=1时,按1.5 mol A、1 mol C作为起始物质,达到平衡后,C的体积分数仍为a |
| B、若在恒温恒容下,当x=2时,将2molC作起始物质,达到平衡后,C的体积分数仍为a |
| C、若在恒温恒压下,当x=3时,1mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为a |
| D、若在恒温恒容下,按0.6mol A、0.3mol B、1.4mol C作起始物质,达到平衡后,C的体积分数仍为a,则x一定为2或3 |
常温下,能被浓硝酸钝化的金属是( )
| A、Mg | B、Fe | C、Cu | D、Ag |
在一固定体积的密闭容器中,加入2mol SO2和1mol O2发生反应2SO2(g)+O2(g)?2SO3(g),达到平衡时,SO2的浓度为w mol/L.若维持容器体积和温度不变,以下列四种配比作为起始物质,达平衡后,SO2的浓度仍为w mol/L的是( )
| A、4mol SO2+2mol O2 |
| B、1mol SO2+1mol O2 |
| C、1mol SO2+1mol O2+1mol SO3 |
| D、1mol SO2+0.5mol O2+1mol SO3 |
在密闭容器中发生下列反应:xA g)+y B(g)?zC(g),平衡时测得A的浓度为 0.5mol/L,保持温度不变,将容器的容积压缩到原来的
,再达平衡时测得A的浓度为 0.8mol/L,下列判断正确的是( )
| 1 |
| 2 |
| A、平衡向逆反应方向移动 |
| B、x+y>z |
| C、B的物质的量增大 |
| D、C的体积分数保持不变 |