题目内容
在一固定体积的密闭容器中,加入2mol SO2和1mol O2发生反应2SO2(g)+O2(g)?2SO3(g),达到平衡时,SO2的浓度为w mol/L.若维持容器体积和温度不变,以下列四种配比作为起始物质,达平衡后,SO2的浓度仍为w mol/L的是( )
| A、4mol SO2+2mol O2 |
| B、1mol SO2+1mol O2 |
| C、1mol SO2+1mol O2+1mol SO3 |
| D、1mol SO2+0.5mol O2+1mol SO3 |
考点:等效平衡
专题:化学平衡专题
分析:在恒温恒容条件下,对于反应2SO2(g)+O2(g)?2SO3(g),由于是气体体积前后不等的反应,所以要使SO2的浓度仍为w mol/L,则必须满足完全等效平衡,按化学计量转化到左边,对应成分的物质的量相同,即满足2mol SO2气体和1mol O2气体,据此判断.
解答:
解:在恒温恒容条件下,对于反应2SO2(g)+O2(g)?2SO3(g),由于是气体体积前后不等的反应,所以要使SO2的浓度仍为w mol/L,则必须满足完全等效平衡,按化学计量转化到左边,对应成分的物质的量相同,即满足2mol SO2气体和1mol O2气体,
A、开始为4mol SO2+2mol O2,与原平衡的反应物的量不等,故A错误;
B、开始为1 mol SO2+1 mol O2,与原平衡的反应物的量不等,故B错误;
C、开始为1 mol SO2+1.0 mol O2+1 mol SO3,转化到左边,相当于2mol SO2+1.5mol O2,与原平衡的反应物的量不等,故C错误;
D、开始为1 mol SO2+0.5 mol O2+1.0 mol SO3,转化到左边,相当于2mol SO2+1mol O2,与原平衡的反应物的量相等,故D正确;
故选D.
A、开始为4mol SO2+2mol O2,与原平衡的反应物的量不等,故A错误;
B、开始为1 mol SO2+1 mol O2,与原平衡的反应物的量不等,故B错误;
C、开始为1 mol SO2+1.0 mol O2+1 mol SO3,转化到左边,相当于2mol SO2+1.5mol O2,与原平衡的反应物的量不等,故C错误;
D、开始为1 mol SO2+0.5 mol O2+1.0 mol SO3,转化到左边,相当于2mol SO2+1mol O2,与原平衡的反应物的量相等,故D正确;
故选D.
点评:本题考查化学平衡计算、等效平衡等,难度中等,清楚等效平衡规律是解题的关键.

练习册系列答案
相关题目
取等质量的铝粉分别与足量的稀硫酸或氢氧化钠溶液反应,所得氢气的体积在同样条件下相比( )
| A、与酸反应产生的氢气多 |
| B、与碱反应产生的氢气多 |
| C、一样多 |
| D、不知道铝粉的质量,无法比较 |
下列说法错误的是( )
| A、制取肥皂时,常常加入少量乙醇,目的是加快皂化反应 |
B、海水提镁的主要步骤为: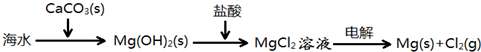 |
| C、工业上将二氧化碳和氨气通入食盐水中制的碳酸氢钠,再煅烧碳酸氢钠使其转化为碳酸钠 |
| D、用蒸馏法便可分离苯和溴苯 |
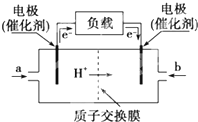 如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列有关该电池的说法错误的是( )
如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列有关该电池的说法错误的是( )| A、右边的电极为电池的负极,b处通入的是空气 |
| B、左边的电极为电池的负极,a处通入的是甲醇 |
| C、电池负极的反应式为:2CH3OH+2H2O-12e-═2CO2↑+12H+ |
| D、电池正极的反应式为:3O2+12H++12e-═6H2O |
下列叙述的两个量,一定相等的是( )
| A、等质量的铝分别与盐酸和氢氧化钠溶液反应生成氢气的物质的量 |
| B、1 mol/L KI与0.5 mol/L K2CO3溶液中的K+数目 |
| C、质量比为3:4的金刚石和石墨中的碳碳键数目 |
| D、常温下,pH均为3的HNO3与Fe(NO3)3溶液中,由水电离产生的c(H+) |
在一定温度下容积恒定的密闭容器中,充入2mol A、1mol B和4mol M,发生如下反应:2A(g)+B(g)+M(s)═xC(g),达到平衡后C的体积分数为a%.若在相同条件下,x分别为2或3时,均按起始物质的量为0.6mol A、0.3mol B、1.4mol C、2mol M充入容器中,分别达到平衡状态,两平衡状态中C的体积分数为( )
| A、两者都小于a% |
| B、两者都大于a% |
| C、两者都等于a% |
| D、无法确定 |
金属的下列性质中与金属晶体结构无关的是( )
| A、导电性 | B、化学反应中易失去电子 |
| C、延展性 | D、硬度 |
分子式为C4H8Cl2,结构中仅含一个-CH3的同分异构体共有(不考虑立体异构( )
| A、6种 | B、5种 | C、4种 | D、3种 |
在等质量的SO2和SO3中,含有的S原子的个数之比为( )
| A、4:5 | B、5:4 |
| C、1:1 | D、3:2 |