题目内容
19.下列有关Na2CO3和NaHCO3的叙述中,正确的是( )| A. | 受热时,NaHCO3比Na2CO3容易分解 | |
| B. | NaHCO3俗名苏打,Na2CO3俗名纯碱 | |
| C. | NaHCO3溶液显酸性,Na2CO3溶液显碱性 | |
| D. | NaHCO3和Na2CO3各1mol分别与过量盐酸反应,产生CO2的质量不同 |
分析 A.根据NaHCO3不稳定,加热易分解进行比较;
B.NaHCO3俗名小苏打,Na2CO3俗名纯碱;
C.都是强碱弱酸盐,水解都显碱性;
D.Na2CO3和NaHCO3分别能与盐酸反应,放出CO2.等物质的量的Na2CO3和NaHCO3分别与过量盐酸反应,放出CO2一样多.
解答 解:A.NaHCO3不稳定,加热易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,碳酸钠较稳定,一般条件下加热不分解,故A正确;
B.NaHCO3俗名小苏打,Na2CO3俗名纯碱,故B错误;
C.碳酸钠和碳酸氢钠都是强碱弱酸盐,水解都显碱性,故C错误;
D.NaHCO3和Na2CO3都可以与盐酸反应,Na2CO3+2HCl=2NaCl+H2O+CO2↑(盐酸过量),NaHCO3+HCl=NaCl+H2O+CO2↑,等物质的量的Na2CO3和NaHCO3分别与过量盐酸反应,放出CO2质量相等,故D错误.
故选A.
点评 本题考查了Na2CO3和NaHCO3性质的比较,题目难度中等,注意熟练掌握Na2CO3和NaHCO3的性质,明确碳酸钠和碳酸氢钠的热稳定性及相互转化的反应原理.

练习册系列答案
相关题目
11.某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气.为了验证哪位同学的判断正确,丙同学设计了如图1所示实验装置(锌与浓硫酸共热时产生的气体为X,气体发生装置略去).试回答:
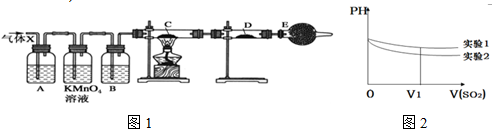
(1)上述反应中生成二氧化硫的化学方程式为Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O.
(2)乙同学认为还可能产生氢气的理由是在Zn与浓H2SO4反应过程中,H2SO4被消耗且有水生成,H2SO4浓度逐渐减小,变成稀硫酸,Zn与稀H2SO4反应生成H2.
(3)A中加入的试剂可能是品红溶液,作用是检验SO2;B中加入的试剂可能是浓H2SO4,作用是吸收水蒸气;
(4)可以证明气体X中含有氢气的实验现象是:C中:黑色(CuO)粉末变成红色(Cu),D中:白色粉末变成蓝色.
(5)II.该小组同学将收集的SO2气体通入0.1mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
该小组设计实验验证了假设一,
(5)请在下表空白处填写相关实验现象
(6)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图2,实验1中溶液pH变小的原因是SO2溶于水后生成H2SO3,亚硫酸显酸性,故pH值减小V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2H2O+2NO3- 2NO+4H++3SO42-;.
2NO+4H++3SO42-;.

(1)上述反应中生成二氧化硫的化学方程式为Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O.
(2)乙同学认为还可能产生氢气的理由是在Zn与浓H2SO4反应过程中,H2SO4被消耗且有水生成,H2SO4浓度逐渐减小,变成稀硫酸,Zn与稀H2SO4反应生成H2.
(3)A中加入的试剂可能是品红溶液,作用是检验SO2;B中加入的试剂可能是浓H2SO4,作用是吸收水蒸气;
(4)可以证明气体X中含有氢气的实验现象是:C中:黑色(CuO)粉末变成红色(Cu),D中:白色粉末变成蓝色.
(5)II.该小组同学将收集的SO2气体通入0.1mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
该小组设计实验验证了假设一,
(5)请在下表空白处填写相关实验现象
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | 假设一成立 | |
| 实验2:在盛有不含O2的25ml0.1mol/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 |
 2NO+4H++3SO42-;.
2NO+4H++3SO42-;.
12.我国油气资源匮乏而煤储量相对丰富.将煤转化为水煤气(CO、H2),不可能产生的效果是( )
| A. | 得到相对清洁的能源 | B. | 提高了能源利用率 | ||
| C. | 增加了单位质量煤的热值 | D. | 便于管道输送 |
7.在容积不变的密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g),反应达平衡状态的标志是( )
①单位时间内生成n mol N2的同时生成2n mol NH3
②用N2、H2、NH3的物质的量浓度变化表示的反应速率比为1:3:2的状态
③2v(H2)正=3v(NH3)逆
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态.
①单位时间内生成n mol N2的同时生成2n mol NH3
②用N2、H2、NH3的物质的量浓度变化表示的反应速率比为1:3:2的状态
③2v(H2)正=3v(NH3)逆
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态.
| A. | ①③④ | B. | ②③⑤ | C. | ①③⑤ | D. | ①②③④⑤ |
14.下列反应可用离子方程式“H++OH-=H2O”表示的是( )
| A. | H2SO4溶液与Ba(OH)2溶液混合 | B. | HCl与Ca(OH)2溶液混合 | ||
| C. | HNO3溶液与氨水混合 | D. | NaHCO3溶液与NaOH溶液混合 |
11.KMnO4和MnO2都是重要化学物质,在实验室可以做氧化剂和催化剂,某学习小组对两种物质的制备和性质探究如下:
I.MnO2的制备:
该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如图:
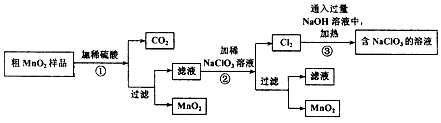
请回答下列问题:
(1)第①步操作中,生成CO2的化学方程式为MnCO3+H2SO4=MnSO4+H2O+CO2↑.
(2)第②步操作中,NaClO3氧化MnSO4的离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+.
(3)第③步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的ad(填序号).
a.NaCl b.NaClO c.NaClO4 d.NaOH
(4)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤.洗涤沉淀所用的玻璃仪器有:烧杯、漏斗、玻璃棒,判断是否洗涤干净可选用的试剂是BaCl2(填化学式).
(5)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为1:3.
(6)工业上可以以石墨为电极电解酸化的硫酸锰制取二氧化锰,该过程的阳极反应式为Mn2+-2e-+2H2O=MnO2+4H+.
II.KMnO4的制备和性质:
(7)实验室由二氧化锰制备高锰酸钾可分二步进行:
第一步:MnO2与KOH共熔并通入氧气:2MnO2+4KOH+O2=2K2MnO4+2H2O
第二步:通入CO2,可使K2MnO4发生歧化反应生成KMnO4和MnO2.
第二步完成反应时,转化为KMnO4的K2MnO4占其全部的百分率约为66.7%(精确到0.1%)
(8)该小组同学为了探究KMnO4溶液和Na2C2O4溶液的反应过程,将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如表:
下列说法中错误的是( )
①请将MnO4-氧化C2O42-的离子方程式补充完整:
2MnO4-+C2O42-+16H+=2Mn2++10CO2↑+8H2O
②请分析KMnO4溶液褪色时间变化的可能原因反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好.
I.MnO2的制备:
该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如图:

请回答下列问题:
(1)第①步操作中,生成CO2的化学方程式为MnCO3+H2SO4=MnSO4+H2O+CO2↑.
(2)第②步操作中,NaClO3氧化MnSO4的离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+.
(3)第③步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的ad(填序号).
a.NaCl b.NaClO c.NaClO4 d.NaOH
(4)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤.洗涤沉淀所用的玻璃仪器有:烧杯、漏斗、玻璃棒,判断是否洗涤干净可选用的试剂是BaCl2(填化学式).
(5)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为1:3.
(6)工业上可以以石墨为电极电解酸化的硫酸锰制取二氧化锰,该过程的阳极反应式为Mn2+-2e-+2H2O=MnO2+4H+.
II.KMnO4的制备和性质:
(7)实验室由二氧化锰制备高锰酸钾可分二步进行:
第一步:MnO2与KOH共熔并通入氧气:2MnO2+4KOH+O2=2K2MnO4+2H2O
第二步:通入CO2,可使K2MnO4发生歧化反应生成KMnO4和MnO2.
第二步完成反应时,转化为KMnO4的K2MnO4占其全部的百分率约为66.7%(精确到0.1%)
(8)该小组同学为了探究KMnO4溶液和Na2C2O4溶液的反应过程,将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如表:
| 起始加入量(mol) | 平衡时 | ||||
| A | B | C | A或C转化率(%) | C的物质的量分数(%) | 放出或吸收热量(KJ) |
| 1 | 1 | 0 | α1 | φ1 | Q1 |
| 0 | 0 | 2 | α2 | φ2 | Q2 |
| 2 | 2 | 0 | α2 | φ3 | Q3 |
①请将MnO4-氧化C2O42-的离子方程式补充完整:
2MnO4-+C2O42-+16H+=2Mn2++10CO2↑+8H2O
②请分析KMnO4溶液褪色时间变化的可能原因反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好.
8.某学生记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热△H=-51.8kJ/mol.
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
9.下列离子方程式书写正确的是( )
| A. | C12与水反应:C12+H2O═2H++Cl-+ClO- | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | Fe跟HCl溶液反应:Fe+2H+═Fe2++H2↑ | |
| D. | BaCO3与盐酸反应:CO32-+2 H+═H2O+CO2↑ |