题目内容
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
(1)该电池的负极材料是 .电池工作时,电子流向 (填“正极”或“负极”).
(2)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是 .若电解电路中通过2mol电子,MnO2的理论产量为 .
(1)该电池的负极材料是
(2)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)锌锰原电池中负极材料为活泼金属Zn,MnO2为正极,电池工作时电子从负极经外电路流向正极;
(2)电解酸化的MnSO4溶液时,根据离子的放电顺序,阴极上首先放电的是H+,电极反应式为:2H++2e-=H2↑,阳极反应式为:MnSO4-2e-+2H2O═MnO2+SO42-+4H+,若电路中通过2mol电子产生1molMnO2,质量为87g.
(2)电解酸化的MnSO4溶液时,根据离子的放电顺序,阴极上首先放电的是H+,电极反应式为:2H++2e-=H2↑,阳极反应式为:MnSO4-2e-+2H2O═MnO2+SO42-+4H+,若电路中通过2mol电子产生1molMnO2,质量为87g.
解答:
解:(1)负极上是失电子的,则Zn失电子为负极,电子由负极流向正极,故答案为:Zn(或锌);正极;
(2)阴极上得电子,发生还原反应,H+得电子生成氢气,即2H++2e-→H2↑,因为MnSO4~MnO2~2e-,通过2mol电子产生1molMnO2,其质量为87g.故答案为:2H++2e-→H2;87g.
(2)阴极上得电子,发生还原反应,H+得电子生成氢气,即2H++2e-→H2↑,因为MnSO4~MnO2~2e-,通过2mol电子产生1molMnO2,其质量为87g.故答案为:2H++2e-→H2;87g.
点评:本题是将典型的实验知识与原电池原理、电解原理相融合的题型,涉及了电极材料分析、电解液净化及相关电化学计算等内容,具有较宽的知识覆盖面.学习中要电化学基础知识掌握扎实.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
下列说法正确的是( )
| A、室温下,pH为11的氨水与pH为3的盐酸等体积混合,溶液呈中性 |
| B、在0.1 mol/L(NH4)2Fe(SO4)2溶液中:c(H+)+c(NH4+)+c(Fe2+)═c(OH-)+c(SO42-) |
| C、向醋酸溶液中加入适量醋酸钠,所得酸性溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、0.2mo1?L-1的Na2CO3溶液:c(OH-)═c(HCO3-)+c(H+)+2c(H2CO3) |
PM2.5细颗粒物含有的毒性物质来源之一是汽车尾气排放.通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx+CO
N2+CO2,下列关于此反应的说法中,不正确的是( )
| 催化剂 |
| A、所涉及元素中原子半径:C>N>O |
| B、等物质的量N2和CO2中,共价键的个数比为3:4 |
| C、氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
| D、当x=2时,每生成1mol N2,转移电子数为4mol |
 在一定温度下有pH均为2的X、Y、Z三种不同的一元酸各5mL,分别加水稀释到5000mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
在一定温度下有pH均为2的X、Y、Z三种不同的一元酸各5mL,分别加水稀释到5000mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )| A、若X、Y、Z都是弱酸,则a的值一定小于5 |
| B、三种酸的原来的浓度大小为X>Y>Z |
| C、稀释后X溶液中水的电离程度最小 |
| D、完全中和原X、Y两溶液时,消耗同浓度NaOH的体积 V(X)>V(Y) |
常见的一种锂离子电池的工作原理为LiCoO2+6C
Li1-xCoO2+LixC6.下列说法正确的是( )
| 充电 |
| 放电 |
| A、充电时,阳极的电极反应式为Li1-xCoO2+xLi+xe-═LiCoO2 |
| B、充电时锂离子由阴极流向阳极 |
| C、放电时,负极的电极反应式为6C+xLi++xe-═Li2C6 |
| D、放电时锂离子由负极流向正极 |
 烯烃分子在一定条件下会发生二分子聚合,其实质是一个分子中饱和碳原子上的一个C-H键断裂,对另一个分子中的双键进行加成.也可以烯烃复分解反应.如:
烯烃分子在一定条件下会发生二分子聚合,其实质是一个分子中饱和碳原子上的一个C-H键断裂,对另一个分子中的双键进行加成.也可以烯烃复分解反应.如:
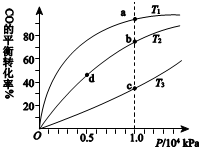 用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示.下列说法正确的是( )
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示.下列说法正确的是( )