题目内容
 烯烃分子在一定条件下会发生二分子聚合,其实质是一个分子中饱和碳原子上的一个C-H键断裂,对另一个分子中的双键进行加成.也可以烯烃复分解反应.如:
烯烃分子在一定条件下会发生二分子聚合,其实质是一个分子中饱和碳原子上的一个C-H键断裂,对另一个分子中的双键进行加成.也可以烯烃复分解反应.如:2CH3-CH=CH2→

CH3CH=CHCH3+CH2=CH2
| 金属卡宾 |
(1)HOCH2CH(CH3)CHO转变成(CH3)2C=CH2须经过
(2)将(CH3)2C=CH2经二分子聚合后的生成物,其主链上有五个碳原子的产物的结构简式为:
(3)在(2)中除了符合上述条件的产物外,还可能有另一种二分子聚合后的生成物,写出生成该生成物的化学方程式:
(4)烯烃复分解反应可以合成其他反应难以合成的物质,制取如图所需要的烯烃为
考点:有机物的合成,有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:(1)HOCH2CH(CH3)CHO转变成(CH3)2C=CH2,先发生消去反应生成CH2=CH(CH3)CHO,再加成生成CH3CH2(CH3)CH2OH,最后发生消去反应;
(2)(CH3)2C=CH2经二分子聚合后的生成物,主链上有五个碳原子,生成(CH3)3CCH2(CH3)C=CH2,该有机物与足量氢气反应后生成(CH3)3CCH2(CH3)CHCH3;
(3)可能有另一种二分子聚合后的生成物,可能发生双键的加成反应,即生成物为(CH3)2CHCH2CH 2C(CH3)=CH2;
(4)烯烃复分解反应合成 ,需要双键和双键C连接2个苯环,以此来解答.
,需要双键和双键C连接2个苯环,以此来解答.
(2)(CH3)2C=CH2经二分子聚合后的生成物,主链上有五个碳原子,生成(CH3)3CCH2(CH3)C=CH2,该有机物与足量氢气反应后生成(CH3)3CCH2(CH3)CHCH3;
(3)可能有另一种二分子聚合后的生成物,可能发生双键的加成反应,即生成物为(CH3)2CHCH2CH 2C(CH3)=CH2;
(4)烯烃复分解反应合成
 ,需要双键和双键C连接2个苯环,以此来解答.
,需要双键和双键C连接2个苯环,以此来解答.解答:
解:(1)HOCH2CH(CH3)CHO转变成(CH3)2C=CH2,先发生消去反应生成CH2=CH(CH3)CHO,再加成生成CH3CH2(CH3)CH2OH,最后发生消去反应,则需要发生的反应为消去反应、加成反应、消去反应,故答案为:消去反应;加成反应;消去反应;
(2)(CH3)2C=CH2经二分子聚合后的生成物,主链上有五个碳原子,生成(CH3)3CCH2(CH3)C=CH2,该有机物与足量氢气反应后生成(CH3)3CCH2(CH3)CHCH3,其名称为 2,2,4-三甲基戊烷,故答案为:(CH3)3CCH2(CH3)C=CH2; 2,2,4-三甲基戊烷;
(3)可能有另一种二分子聚合后的生成物,可能发生双键的加成反应,即生成物为(CH3)2CHCH2CH 2C(CH3)=CH2,该加成反应为2(CH3) 2C=CH2→(CH3)2CHCH2CH 2C(CH3)=CH2,故答案为:2(CH3) 2C=CH2→(CH3)2CHCH2CH 2C(CH3)=CH2;
(4)烯烃复分解反应合成 ,需要双键和双键C连接2个苯环,反应产生的另一种产物是石油裂解气乙烯,则所需要的烯烃为
,需要双键和双键C连接2个苯环,反应产生的另一种产物是石油裂解气乙烯,则所需要的烯烃为
 ,故答案为:
,故答案为: .
.
(2)(CH3)2C=CH2经二分子聚合后的生成物,主链上有五个碳原子,生成(CH3)3CCH2(CH3)C=CH2,该有机物与足量氢气反应后生成(CH3)3CCH2(CH3)CHCH3,其名称为 2,2,4-三甲基戊烷,故答案为:(CH3)3CCH2(CH3)C=CH2; 2,2,4-三甲基戊烷;
(3)可能有另一种二分子聚合后的生成物,可能发生双键的加成反应,即生成物为(CH3)2CHCH2CH 2C(CH3)=CH2,该加成反应为2(CH3) 2C=CH2→(CH3)2CHCH2CH 2C(CH3)=CH2,故答案为:2(CH3) 2C=CH2→(CH3)2CHCH2CH 2C(CH3)=CH2;
(4)烯烃复分解反应合成
 ,需要双键和双键C连接2个苯环,反应产生的另一种产物是石油裂解气乙烯,则所需要的烯烃为
,需要双键和双键C连接2个苯环,反应产生的另一种产物是石油裂解气乙烯,则所需要的烯烃为 ,故答案为:
,故答案为: .
.
点评:本题考查有机物的合成及推断,为高频考点,把握烯烃加成反应及烯烃复分解反应的规律为解答的关键,侧重分析与推断能力的综合考查,题目难度中等.

练习册系列答案
相关题目
在常温常压下,下列各组气体不能大量共存的是( )
| A、N2与H2 |
| B、NO2与NO |
| C、N2与O2 |
| D、NH3与HCl |
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是( )
| A、加入合金的质量不可能为6.4 g |
| B、参加反应的硝酸的物质的量为0.1 mol |
| C、沉淀完全时消耗NaOH溶液的体积为150 mL |
| D、溶解合金时收集到NO气体标准状况下的体积为2.24 L |
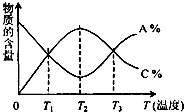 已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是 (两个答案)( )
已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是 (两个答案)( )| A、该反应在T1、T3温度时达到过化学平衡 |
| B、该反应在T2温度时达到过化学平衡 |
| C、该反应的逆反应是吸热反应 |
| D、升高温度,平衡会向正反应方向移动 |
 恒温下,a mol A和b mol B在如图所示活塞可自由滑动的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成n mol C.则下列说法中正确的是( )
恒温下,a mol A和b mol B在如图所示活塞可自由滑动的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成n mol C.则下列说法中正确的是( )| A、物质A、B的转化率之比为a:b |
| B、起始时刻和达平衡后容器中的压强比为(a+b):(a+b-n/2) |
| C、平衡时C的体积分数为n/(a+b-n/2) |
| D、当v正(A)=2v逆(B)时,可判定反应达到平衡 |
己知反应A(s)+B(g)?C(g)+D(g)的化学平衡常数和温度的关系如表下列说法正确的是( )
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 化学平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A、该反应的化学平衡常数表达式为:K=
| ||
| B、该反应为吸热反应 | ||
| C、单位时间内生成B和D的物质的量相等时,该反应处于平衡状态 | ||
| D、其它条件不变时,增大体系的压强,化学平衡常数减小 |