题目内容
16.短周期元素A、B、C、D在周期表中的位置关系如图所示.已知在同周期元素的常见简单离子中,D的离子半径最小,E是周期表中半径最小的原子| A | B | C | |
| D |
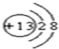
(1)C元素在元素周期表中的位置是第二周期第VIA 族.元素D的离子结构示意图为
(2)B、E两元素按原子数目比1:3和2:4构成分子X和Y,X的电子式为
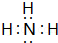 ,Y的结构式为
,Y的结构式为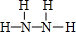
(3)工业上冶炼单质D的化学反应方程式2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
(4)超细DB粉末被应用于大规模集成电路领域.其制作原理为D2C3、B2、A在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:l;其反应的化学方程式为Al2O3+N2+3C $\frac{\underline{\;高温\;}}{\;}$ 2AlN+3CO.
分析 由短周期主族元素A、B、C、D在周期表中的位置,可知A、B、C处于第二周期,D处于第三周期,在同周期元素的常见简单离子中,D的离子半径最小,则D为Al,可推知A为碳、B为氮、C为氧,E是周期表中半径最小的原子,则E为H元素,据此解答.
解答 解:由短周期主族元素A、B、C、D在周期表中的位置,可知A、B、C处于第二周期,D处于第三周期,在同周期元素的常见简单离子中,D的离子半径最小,则D为Al,可推知A为碳、B为氮、C为氧,E是周期表中半径最小的原子,则E为H元素.
(1)C为氧元素,在元素周期表中的位置是:第二周期第VIA 族,元素D为Al,离子结构示意图为  ,
,
故答案为:第二周期第VIA 族; ;
;
(2)N、H两元素按原子数目比1:3和2:4构成分子X和Y,X为NH3,电子式为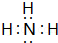 ,Y为N2H4,结构式为
,Y为N2H4,结构式为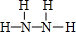 ,
,
故答案为: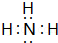 ;
;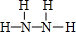 ;
;
(3)工业上电解熔融氧化铝冶炼单质Al,化学反应方程式为:2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,
故答案为:2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;
(4)超细AlN粉末被应用于大规模集成电路领域.其制作原理为Al2O3、N2、碳在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:l,还生成CO,反应的化学方程式为:Al2O3+N2+3C $\frac{\underline{\;高温\;}}{\;}$ 2AlN+3CO,
故答案为:Al2O3+N2+3C $\frac{\underline{\;高温\;}}{\;}$ 2AlN+3CO.
点评 本题考查结构性质位置关系应用,根据元素的位置推断元素是解题的关键,侧重对化学用语的考查,注意对基础知识的理解掌握,难度不大.

| A. | 位于第四周期、第ⅠA 族 | |
| B. | 氢氧化铷是弱碱 | |
| C. | 在钠、钾、铷3种单质中,铷的熔点最高 | |
| D. | 硝酸铷是离子化合物 |
①第3周期 ②第2周期 ③第ⅣA 族 ④第ⅤA族.
| A. | ②④ | B. | ①④ | C. | ①③ | D. | ②③ |
| A. | 从C(石墨)=C(金刚石)△H=+1.9 kJ•mol-1,可知金刚石比石墨更稳定 | |
| B. | 相同条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 | |
| C. | 由H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1,可知含1 mol CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量等于57.3 kJ | |
| D. | 2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ•mol-1 |
| 族 周 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 _.
_.(2)给出的第二周期的几种元素中,原子半径最大的是F (填元素符号).
(3)元素③与⑧的气态氢化物中较稳定的物质是
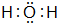 (填该物质的电子式).
(填该物质的电子式).(4)元素⑤与⑥的最高价氧化物的水化物的碱性更强的物质是Mg(OH)2(填化学式).
(5)元素③与⑦能以共价键(填化学键类型)结合成分子晶体(填晶体类型).