题目内容
6.下列离子方程式正确的是( )| A. | 将0.2 mol/L的NH4Al(SO4)2溶液与0.3 mol/L的Ba(OH)2溶液等体积混合:2NH4++Al3++3SO42-+3Ba2++6OH-═Al(OH)3↓+AlO2-+3BaSO4↓+2H2O | |
| B. | 将含有等物质的量溶质的NaHCO3溶液和Ba(OH)2溶液混合:Ba2++HCO${\;}_{3}^{-}$+OH-═BaCO3↓+H2O | |
| C. | 在重铬酸钾溶液中,加酸后溶液变为黄色:Cr2O72-+H2O═2 CrO42-+2H+ | |
| D. | 过量氯水与FeI2溶液作用:2Fe2++2I-+2Cl2═2 Fe3++I2+4Cl- |
分析 A.物质的量比为2:3,反应生成硫酸钡、氢氧化铝、硫酸铵;
B.等物质的量反应生成碳酸钡、水、NaOH;
C.Cr2O72-(橙红色)+H2O?2H++2CrO42-(黄色),为可逆反应;
D.碘离子、亚铁离子均为氧化.
解答 解:A.将0.2 mol/L的NH4Al(SO4)2溶液与0.3 mol/L的Ba(OH)2溶液等体积混合的离子反应为2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓,故A错误;
B.含有等物质的量溶质的NaHCO3溶液和Ba(OH)2溶液混合的离子反应为Ba2++HCO3-+OH-═BaCO3↓+H2O,故B正确;
C.在重铬酸钾溶液中,加酸后Cr2O72-(橙红色)+H2O?2H++2CrO42-(黄色)逆向进行,溶液变为橙红色,故C错误;
D.过量氯水与FeI2溶液作用的离子反应为2Fe2++4I-+3Cl2═2Fe3++2I2+6Cl-,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,注重离子反应的综合训练,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
19.用粗氧化铜(含少量Fe)制取纯净的CuCl2?2H2O的主要过程是:
①将粗氧化铜溶解于稀盐酸中,加热、过滤.调节滤液的pH为3;
②对①所得的滤液按下列步骤进行操作:
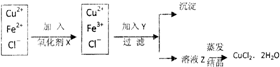
已知:
回答下列问题:
(1)加入氧化剂X的目的是:将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离
本实验最合适的氧化剂X是c(填字母)
a.K2Cr2O7 b.NaClO c.H2O2 d.KMnO4
反应的离子方程式是2H++H2O2+2Fe2+=2Fe3++2H2O.
(2)Y可选:CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3,调节pH3.2≤pH<4.7
除去Fe3+的有关离子方程式为CuO+2H+=Cu2++H2O、Fe3++3H2O=Fe(OH)3+3H+
(3)采用低温减压蒸发结晶的方法得到CuCl?2H2O的晶体,还要在过程中不断通入HCl气体,且不能蒸干.
①将粗氧化铜溶解于稀盐酸中,加热、过滤.调节滤液的pH为3;
②对①所得的滤液按下列步骤进行操作:

已知:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
(1)加入氧化剂X的目的是:将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离
本实验最合适的氧化剂X是c(填字母)
a.K2Cr2O7 b.NaClO c.H2O2 d.KMnO4
反应的离子方程式是2H++H2O2+2Fe2+=2Fe3++2H2O.
(2)Y可选:CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3,调节pH3.2≤pH<4.7
除去Fe3+的有关离子方程式为CuO+2H+=Cu2++H2O、Fe3++3H2O=Fe(OH)3+3H+
(3)采用低温减压蒸发结晶的方法得到CuCl?2H2O的晶体,还要在过程中不断通入HCl气体,且不能蒸干.
16.下列物质中,属于非电解质的是( )
| A. | 氯化氢 | B. | 氢氧化钠 | C. | 酒精 | D. | 氯化钠 |
11.粗碳酸锂(含有Na+、K+、Ca2+等杂质离子)制备高纯碳酸锂的工艺流程如图1:
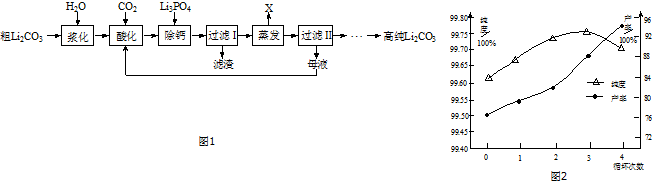
碳酸锂溶解度与温度的关系见下表:
(1)浆料酸化时,温度不宜超过25℃的主要原因是温度越高,碳酸锂、二氧化碳溶解度都越小,减小了反应速率.判断酸化过程已经结束的明显现象为浆料变成澄清溶液.
(2)已知Ksp[Ca3(PO4)2]=2.0×10-29,为使溶液中c(Ca2+)≤2×10-5mol•L-1,c(PO43- )的范围
为c(PO43- )≥5×10-8mol•L-1.
(3)蒸发时主要反应的离子方程式为2Li++2HCO3-=Li2CO3↓+CO2↑+H2O.母液循环次数对纯度、产率的影响如图2所示,循环不宜超过3次的主要原因是循环次数增多,溶液中钠离子、钾离子的浓度会增大,会降低产品的纯度.
(4)为了获得高纯Li2CO3,过滤Ⅱ后的操作为将碳酸锂用热水洗涤2~3次、干燥.

碳酸锂溶解度与温度的关系见下表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(2)已知Ksp[Ca3(PO4)2]=2.0×10-29,为使溶液中c(Ca2+)≤2×10-5mol•L-1,c(PO43- )的范围
为c(PO43- )≥5×10-8mol•L-1.
(3)蒸发时主要反应的离子方程式为2Li++2HCO3-=Li2CO3↓+CO2↑+H2O.母液循环次数对纯度、产率的影响如图2所示,循环不宜超过3次的主要原因是循环次数增多,溶液中钠离子、钾离子的浓度会增大,会降低产品的纯度.
(4)为了获得高纯Li2CO3,过滤Ⅱ后的操作为将碳酸锂用热水洗涤2~3次、干燥.
18.在一密闭容器中有CH4和O2混合气体共20g,放入足量Na2O2用电火花引燃,使其完全反应,Na2O2增重8g,则原混合气体中O2的质量分数是( )
| A. | 80% | B. | 60% | C. | 40% | D. | 33.3% |
15.下列物质中,只含有共价键的物质是( )
| A. | MgCl2 | B. | H2O | C. | Ne | D. | NaOH |