题目内容
16.含SO2的工业尾气可用石灰乳吸收处理,再经氧化制得CaSO4•2H2O(石膏),若处理含SO2 0.224%(体积分数)的尾气1×106 m3(标准状况),假定原料利用率均为100%,理论上可得到石膏的质量为(吨)( )| A. | 17.2 | B. | 1.72 | C. | 1.2 | D. | 0.0172 |
分析 根据二氧化硫的体积分数计算出二氧化硫的体积,再根据二氧化硫与CaSO4•2H2O的转化关系,由质量守恒计算出石膏(CaSO4•2H2O)的质量.
解答 解:由硫元素质量守恒可知二氧化硫与CaSO4•2H2O的微粒数比为1:1,则
SO2-------------CaSO4•2H2O
22.4L 172g
1×109L×0.224% xg
则x=$\frac{1×1{0}^{9}L×0.224%×172g}{22.4}$=1.72×107g=17.2t,
故选A.
点评 本题考查了有关方程式的计算,题目难度不大,明确发生反应实质为解答关键,注意利用元素守恒计算较简单,试题侧重于考查学生的计算能力和分析能力.

练习册系列答案
相关题目
6.下列离子方程式正确的是( )
| A. | 将0.2 mol/L的NH4Al(SO4)2溶液与0.3 mol/L的Ba(OH)2溶液等体积混合:2NH4++Al3++3SO42-+3Ba2++6OH-═Al(OH)3↓+AlO2-+3BaSO4↓+2H2O | |
| B. | 将含有等物质的量溶质的NaHCO3溶液和Ba(OH)2溶液混合:Ba2++HCO${\;}_{3}^{-}$+OH-═BaCO3↓+H2O | |
| C. | 在重铬酸钾溶液中,加酸后溶液变为黄色:Cr2O72-+H2O═2 CrO42-+2H+ | |
| D. | 过量氯水与FeI2溶液作用:2Fe2++2I-+2Cl2═2 Fe3++I2+4Cl- |
7.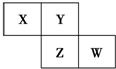 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )| A. | X的最常见气态氢化物的水溶液显碱性 | |
| B. | 最高价氧化物对应水化物的酸性W比Z弱 | |
| C. | Z的单质与氢气反应比Y单质与氢气反应剧烈 | |
| D. | X、W的气态氢化物相互反应,生成物中只含离子键不含共价键 |
4.下列设计的实验方案能达到实验目的是( )
| A. | 配制FeCl3溶液:将FeCl3固体溶于适量热的蒸馏水中,然后冷却至室温 | |
| B. | 制备银氨溶液:在1mL2%的氨水中逐滴加入2%的AgNO3溶液直至过量 | |
| C. | 提纯含有少量苯酚的苯:向含有少量苯酚的苯中加入适量浓溴水,过滤 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mL H2O,向另一支试管中加入2mL 5%H2O2和1mL FeCl3溶液,观察并比较实验现象 |
11.美国Marchetin博士对世界一次能源替代趋势曾作如下预测.有关说法不正确的是( )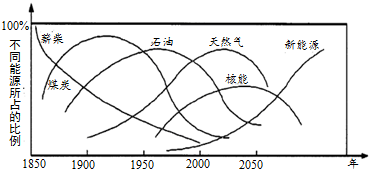

| A. | 太阳能、氢能和生物质能等均属于新能源 | |
| B. | 能源物质在提供能量的同时一定有新核素生成 | |
| C. | 天然气与煤炭、石油及薪柴相比,具有热值高、洁净等优势 | |
| D. | 煤、石油及天然气蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
1.下列有关海水综合利用的说法正确的是( )
| A. | 利用电解的方法可以从海水中获取淡水 | |
| B. | 海水中含有溴元素,只需经过蒸馏等物理变化就可以得到溴单质 | |
| C. | 海水蒸发制海盐的过程只发生了化学变化 | |
| D. | 从海水中提镁时,利用海滩上的贝壳制Ca(OH)2 |
5.下列关于同分异构体数目的叙述不正确的是( )
| A. | 甲苯苯环上的1 个氢原子被含3 个碳原子的烷基取代,所得产物有6 种 | |
| B. | 已知丙烷的二氯代物有4 种异构体,则其六氯代物的异构体数目也为4 种 | |
| C. | 含有5 个碳原子的某饱和链烃,其一氯代物有3 种 | |
| D. | 菲的结构为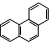 ,它与硝酸反应,可生成5 种一硝基取代物 ,它与硝酸反应,可生成5 种一硝基取代物 |
6.a、b、c、d均为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,b与d同主族.下列叙述正确的是( )
| A. | a分别与b、c、d形成的二元化合物中a的化合价均为+1 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | a与b形成的化合物中一定只有共价键,b与c形成的化合物中一定只有离子键 | |
| D. | 原子半径大小顺序d>c>b>a |