题目内容
1.(1)在①CaCl2、②KOH、③CO2、④NaHSO4、⑤Na2O2、⑥N2中,只含有离子键的是(填序号,下同)①,只含有极性键的是④,含有非极性键的离子化合物是⑤.(2)将NaHSO4溶于水,破坏的化学键是离子键、共价键,I2 升华破坏的是分之间作用力.
分析 (1)一般来说,活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物;
(2)将NaHSO4溶于水,发生电离,生成钠离子、氢离子、硫酸根离子;I2 升华分子不变,化学键不变.
解答 解:(1)①CaCl2只含离子键,为离子化合物;
②KOH含离子键和O-H极性共价键,为离子化合物;
③CO2只含极性共价键,为共价化合物;
④NaHSO4含离子键和极性共价键,为离子化合物;
⑤Na2O2含离子键和O-O非极性共价键,为离子化合物;
⑥N2中只含非极性键,为单质,则
只含有离子键的是①,只含有极性键的是④,含有非极性键的离子化合物是⑤,
故答案为:①;④;⑤;
(2)将NaHSO4溶于水,发生电离,生成钠离子、氢离子、硫酸根离子,则离子键、共价键破坏;I2 升华分子不变,化学键不变,则只破坏分之间作用力,
故答案为:离子键、共价键;分之间作用力.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
14.生活中的问题常涉及化学知识,下列过程不涉及化学变化的是( )
| A. | 用食醋除去暖瓶内的水垢 | B. | 用四氯化碳擦去圆珠笔油渍 | ||
| C. | 用糯米饭、酒曲等自制甜酒酿 | D. | 用烧碱清除炊具上残留的油污 |
11.在标准状况下,下列各组气体混合后,所得气体的平均摩尔质量可能为40g•mol-1的是( )
| A. | Cl2和HCl | B. | N2和O2 | C. | SO2和CO2 | D. | CO2和O2 |
18.仅能在水溶液中导电的电解质是( )
| A. | 亚硫酸钠 | B. | 酒精 | C. | 氢氧化钾 | D. | 氯化氢 |
6.下列离子方程式正确的是( )
| A. | 将0.2 mol/L的NH4Al(SO4)2溶液与0.3 mol/L的Ba(OH)2溶液等体积混合:2NH4++Al3++3SO42-+3Ba2++6OH-═Al(OH)3↓+AlO2-+3BaSO4↓+2H2O | |
| B. | 将含有等物质的量溶质的NaHCO3溶液和Ba(OH)2溶液混合:Ba2++HCO${\;}_{3}^{-}$+OH-═BaCO3↓+H2O | |
| C. | 在重铬酸钾溶液中,加酸后溶液变为黄色:Cr2O72-+H2O═2 CrO42-+2H+ | |
| D. | 过量氯水与FeI2溶液作用:2Fe2++2I-+2Cl2═2 Fe3++I2+4Cl- |
13.氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3═bO2↑+cCl2↑+dHClO4+eH2O.下列有关说法正确的是( )
| A. | 由反应可确定:氧化产物是O2 | |
| B. | 若氯酸分解所得混合气体lmol混合气体质量为45g,则反应方程式可表示为:3HClO3═2O2↑+C12↑+HClO4+H2O | |
| C. | 由非金属性Cl>S,可推知酸性HClO3>H2SO4 | |
| D. | 若化学计量数a=8,b=3,则该反应转移电子数为8e- |
10.下列卤代烃中,既能发生消去反应又能发生水解反应的是( )
| A. | 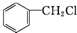 | B. | 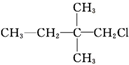 | C. | CH3CHBrCH3 | D. | 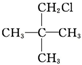 |
11.美国Marchetin博士对世界一次能源替代趋势曾作如下预测.有关说法不正确的是( )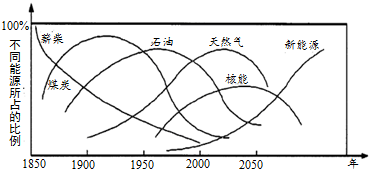

| A. | 太阳能、氢能和生物质能等均属于新能源 | |
| B. | 能源物质在提供能量的同时一定有新核素生成 | |
| C. | 天然气与煤炭、石油及薪柴相比,具有热值高、洁净等优势 | |
| D. | 煤、石油及天然气蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
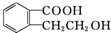 ,它可以通过不同的反应得到下列物质:
,它可以通过不同的反应得到下列物质: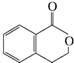 、C.
、C.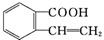 、D.
、D.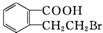 .
. .
. 、
、 .
.